题目内容
用蘸有浓氨水的玻璃棒靠近下列各浓酸时,均有白烟产生的一组是( )
| A、H2SO4、HNO3 |
| B、HCl、HNO3 |
| C、HCl、H2SiO3、 |
| D、HCl、H2SO4 |
考点:氨的化学性质
专题:氮族元素
分析:蘸有浓氨水的玻棒靠近下列各浓酸时,产生白烟,说明酸易挥发,能在空气中形成小颗粒,以此解答该题.
解答:
解:蘸有浓氨水的玻棒靠近下列各浓酸时,产生白烟,说明酸易挥发,能在空气中形成小颗粒,则
HCl、HNO3三种酸都易挥发,与浓氨水反应均有白烟产生,而浓H2SiO3、H2SO4为难挥发性的酸,不能形成白烟,故选B.
HCl、HNO3三种酸都易挥发,与浓氨水反应均有白烟产生,而浓H2SiO3、H2SO4为难挥发性的酸,不能形成白烟,故选B.
点评:本题考查氨气的性质,题目难度不大,注意能形成的白烟的酸必定是易挥发的酸的这一特点.

练习册系列答案
相关题目
 有MgSO4、AlCl3的混合溶液,向其中不断加入NaOH溶 液,得到的沉淀量与加入的NaOH溶液体积的关系如图所示,则原溶液中Cl-与SO42-物质的量浓度之比为( )
有MgSO4、AlCl3的混合溶液,向其中不断加入NaOH溶 液,得到的沉淀量与加入的NaOH溶液体积的关系如图所示,则原溶液中Cl-与SO42-物质的量浓度之比为( )| A、3:2 | B、2:3 |
| C、1:2 | D、2:1 |
下列各组离子或物质能够大量共存的是( )
| A、无色溶液中:MnO4-、Na+、SO42-、HCO3- |
| B、氯水中:CO32-、NO3-、SO42-、Na+ |
| C、常温常压下:NH3、O2、H2、CO2 |
| D、使酚酞变红的溶液中:K+、Cu2+、Cl-、NO3- |
下列表述正确的是( )
| A、100℃时,0.1 mol?L-1 HCl和NaOH溶液的pH分别为1和13 |
| B、将pH=4的醋酸溶液加水稀释后,溶液中所有离子的浓度均降低 |
| C、等体积、等pH的HCl和CH3COOH溶液分别与NaOH溶液反应,CH3 COOH消耗NaOH的物质的量多 |
| D、在滴有酚酞溶液的氨水中,加入NH4Cl至溶液无色,此时溶液一定显中性 |
下列说法不正确的是( )
①形成化学键的过程一定是化学变化
②离子化合物中一定含有金属元素
③物质有阴离子必有阳离子
④含有金属元素的离子一定为阳离子
⑤单质中一定含有共价键
⑥干冰升华破坏化学键
⑦HCI溶于水中电离出H+和Cl-,因此HCl中含有离子键.
①形成化学键的过程一定是化学变化
②离子化合物中一定含有金属元素
③物质有阴离子必有阳离子
④含有金属元素的离子一定为阳离子
⑤单质中一定含有共价键
⑥干冰升华破坏化学键
⑦HCI溶于水中电离出H+和Cl-,因此HCl中含有离子键.
| A、①②④⑤⑥⑦ |
| B、②③⑤⑦ |
| C、③⑤⑥⑦ |
| D、①②③④⑤⑥ |
可逆反应4CO+2NO2═4CO2+N2达到化学平衡时,下列说法正确的是( )
| A、反应混合气体的颜色不再变化 |
| B、CO、CO2两种物质浓度一定相等 |
| C、CO和NO2 全部变成CO2和N2 |
| D、升高温度,正反应速率增大,逆反应速率则减小 |
下列关于工业生产的说法中正确的是( )
| A、氯碱工业中阳离子交换膜的主要作用是防止氯气和氢气以及氢氧化钠反应 |
| B、硫酸工业中合成SO3通常采用常压,是因为常压比高压更有利于SO3的生成 |
| C、电解精炼铜时,纯铜作为阳极,粗铜作为阴极 |
| D、工业合成氨通常采用500℃的高温主要是为了提高氮气的转化率 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、4 4 g CO2气体中所含原子数为2 NA |
| B、常温常压下,22.4 L氢气所含原子数为2 NA |
| C、1 L mo l?L-1的硫酸钠溶液中钠离子数为2 NA |
| D、在Cl2参与的反应中,1 mol Cl2得到的电子数一定是2NA |
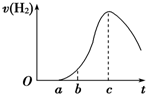 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题: