题目内容
13.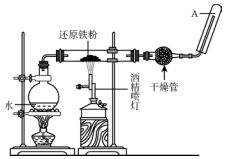 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”.请回答该实验中的问题.
(1)写出该反应的化学方程式3Fe+4H2O (g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(2)实验前必须对整套装置进行的操作是检验装置的气密性.
(3)圆底瓶中盛装的物质可以是水,作用是为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气.
(4)干燥管中盛装的物质可以是碱石灰,作用是除去反应产生的H2中的水蒸气.
(5)试管中收集到的气体是氢气,如果要在A处玻璃管口处点燃该气体,则必须该气体进行验纯,这一操作的目的是防止点燃时,氢气因含有氧气而爆炸.
分析 (1)铁与水蒸气在高温下反应生成物是四氧化三铁和氢气;
(2)实验前必须对整套装置进行气密性检查;
(3)根据反应物为水蒸气与铁解答;
(4)干燥管内固体干燥剂一般用无水氯化钙或固体氢氧化钠和碱石灰等,要注意干燥剂不能和被干燥的物质反应;
(5)点燃氢气前一定要检验纯度,防止发生爆炸.
解答 解:(1)铁与水蒸气在高温下反应生成物是四氧化三铁和氢气,反应方程式为:3Fe+4H2O (g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O(g) $\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(2)实验前必须对整套装置进行气密性检查,故答案为:检验装置的气密性;
(3)因为反应物为水蒸气与铁,所以圆底烧瓶中是水,这里加热的目的就是提供水蒸气,
故答案为:水;为硬质玻璃管内Fe与水蒸气的反应实验提供持续不断的水蒸气;
(4)干燥氢气可以用碱石灰干燥剂,故答案为:碱石灰;除去反应产生的H2中的水蒸气;
(5)铁与水蒸气发生氧化还原反应生成氢气,点燃氢气前一定要检验纯度,防止发生爆炸;
故答案为:氢气;验纯;防止点燃时,氢气因含有氧气而爆炸.
点评 本题为铁及其化合物的性质实验,掌握铁和水蒸气反应的原理和产物的检验是解答的关键,题目难度不大.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
3.肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,反应生成N2和水蒸气.
已知:N2(g)+2O2(g)=N2O4(g);△H=+a kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-b kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
已知:N2(g)+2O2(g)=N2O4(g);△H=+a kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-b kJ/mol
下列表示肼和N2O4反应的热化学方程式,正确的是( )
| A. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-(b+a) kJ/mol | |
| B. | N2H4(g)+$\frac{1}{2}$N2O4(g)=$\frac{3}{2}$N2(g)+2H2O(g);△H=-(2b+a)kJ/mol | |
| C. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-(a-2b) kJ/mol | |
| D. | 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-(b-a) kJ/mol |
4.下列化学试剂不能用于鉴别溴蒸气和二氧化氮的是( )
| A. | 四氯化碳 | B. | 硝酸银溶液 | C. | 淀粉KI试纸 | D. | 水 |
1.在两个恒容的密闭容器中进行下列两个可逆反应:
(甲)2NO2(g)?2NO(g)+O2(g)
(乙)H2(g)+l2(g)?2Hl(g)能够表明(甲)、(乙)俩个反应都达到了化学平衡状态的是( )
(甲)2NO2(g)?2NO(g)+O2(g)
(乙)H2(g)+l2(g)?2Hl(g)能够表明(甲)、(乙)俩个反应都达到了化学平衡状态的是( )
| A. | 恒温时压强不再改变的状态 | |
| B. | 体系温度不在改变的状态 | |
| C. | 恒温时混合气体的密度不再改变的状态 | |
| D. | 混合气体的平均相对分子质量不再改变的状态 |
18.实验室下列物质的保存方法中,不正确的是( )
| A. | 金属钠保存在煤油中 | |
| B. | 铝片放在不密封的容器里 | |
| C. | 硫酸亚铁溶液保存在加有少量铁粉的试剂瓶中 | |
| D. | 氢氧化钠溶液盛装在玻璃塞的试剂瓶中 |
5.下列关于自然界氮循环(如图)的说法不正确的是( )


| A. | 工业合成氮属于人工固氮 | |
| B. | 含氮无机物和含氮有机物可以相互转化 | |
| C. | 氮的固定不一定是化学变化 | |
| D. | 碳、氢、氧三种元素也参与了氮循环 |

 ,
, ,
, .
.