题目内容
甲烷(CH4)与氧气(O2)以物质的量之比1:2混合时极易爆炸,关于该混合气体下列叙述正确的是( )
| A、分子数之比为 1:1 |
| B、原子数之比为5:4 |
| C、质量之比为1:1 |
| D、摩尔质量之比为1:4 |
考点:物质的量的相关计算
专题:
分析:A.同温同压下,甲烷(CH4)与氧气(O2)的物质的量之比等于分子数之比;
B.1mol甲烷(CH4)中含有5mol原子,1mol氧气(O2)含有2mol原子;
C.根据m=nM计算;
D.根据摩尔质量在数值上和相对分子质量相等,单位为g/mol计算.
B.1mol甲烷(CH4)中含有5mol原子,1mol氧气(O2)含有2mol原子;
C.根据m=nM计算;
D.根据摩尔质量在数值上和相对分子质量相等,单位为g/mol计算.
解答:
解:A.甲烷(CH4)与氧气(O2)以物质的量之比1:2,同温同压下,二者物质的量之比等于分子数之比为 1:2,故A错误;
B.甲烷(CH4)与氧气(O2)以物质的量之比1:2,原子数之比为1×5:2×2=5:4,故B正确;
C.甲烷(CH4)与氧气(O2)以物质的量之比1:2,设物质的量分别为1mol、2mol,根据m=nM,质量之比为1mol×16g/mol:2mol×32g/mol=1:4,故C错误;
D.根据摩尔质量的单位为g/mol,在数值上等于该物质的相对原子质量或相对分子质量,因此CH4的摩尔质量为:16g/mol,O4的摩尔质量为:32g/mol,摩尔质量之比为1:2,故D错误;
故选B.
B.甲烷(CH4)与氧气(O2)以物质的量之比1:2,原子数之比为1×5:2×2=5:4,故B正确;
C.甲烷(CH4)与氧气(O2)以物质的量之比1:2,设物质的量分别为1mol、2mol,根据m=nM,质量之比为1mol×16g/mol:2mol×32g/mol=1:4,故C错误;
D.根据摩尔质量的单位为g/mol,在数值上等于该物质的相对原子质量或相对分子质量,因此CH4的摩尔质量为:16g/mol,O4的摩尔质量为:32g/mol,摩尔质量之比为1:2,故D错误;
故选B.
点评:本题考查物质的量计算、阿伏伽德罗定律及推论,题目难度不大,注意理解阿伏伽德罗定律及推论以及相关公式的熟练应用.

练习册系列答案
相关题目
下列装置用于实验室以硫酸铝制取一定量Al2O3,能达到实验目的是 ( )
A、 称取样品 |
B、 样品溶解 |
C、 氢氧化铝沉淀过滤 |
D、 灼烧氢氧化铝沉淀 |
在浩瀚的大海里蕴藏着丰富的化学资源.海水的综合利用是当前非常重要的一个课题.下列有关说法正确的是( )
| A、海水中含量最高的是Na元素和Cl元素 | ||||||
| B、海水晒盐的原理与化学实验中的蒸发操作相似 | ||||||
| C、为了消除碘缺乏病,我国政府规定在食盐中必须加入一定量的I2 | ||||||
D、海水提镁可以通过以下步骤进行:海水
|
某实验需要470mL0.4mol?L-1NaOH溶液,配制该溶液时,用托盘天平称取NaOH固体的质量应为( )
| A、8.0g | B、7.5g |
| C、4.0g | D、7.52g |
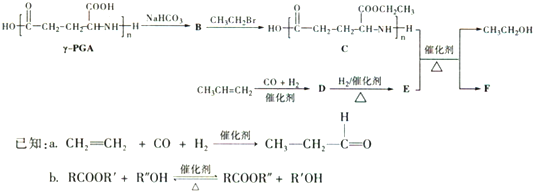
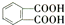 )反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一.DBP有多种同分异构体,其中符合下列条件的DBP的同分异构体有
)反应生成的产物DBP(C16H22O4)是广泛使用的增塑剂之一.DBP有多种同分异构体,其中符合下列条件的DBP的同分异构体有

 互为同分异构,有一苯环且苯环上有互为对位的2个取代基,并能与NaOH反应的有机物不止一种,写出其中一种的结构简式:
互为同分异构,有一苯环且苯环上有互为对位的2个取代基,并能与NaOH反应的有机物不止一种,写出其中一种的结构简式:

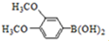 与化合物
与化合物 在一定条件可发生类似反应①的反应,其产物的结构简式为
在一定条件可发生类似反应①的反应,其产物的结构简式为