��Ŀ����
����Ŀ��ƫ����þ�ڻ��������Ͳ��ϡ��������������Ҫ����;��������[��Ҫ�ɷ���MgO��52.1%),����Fe2O3��FeO��Al2O3��SiO2������]Ϊԭ������Ʊ�ƫ����þ������������ͼ��ʾ��
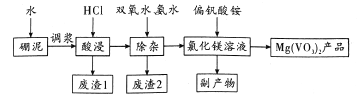
�ش��������⣺
(l)Mg(VO3)2 ��V�Ļ��ϼ�Ϊ_____,������ĵ���ʽΪ_______��
(2�����ʱ����Ӧ�¶��������80�棬��ʵ���ҿɲ�ȡ�Ĵ�ʩΪ______��д�������������Һ�д��ڵĽ���������_______������1����������_______������������Ϣ�����о�����ҪӦ�á�
(3)�����ӡ����̼���˫��ˮ��Ŀ����_______�������ӷ���ʽ��ʾ�����˹�����ʹFe3+��Al3+Ũ�Ⱦ�С��l��10-6mol��L-1���������������pH��ΧΪ__________[��֪Ksp[Fe(OH)3]= 1��10-39, Ksp[Al(OH)]=1��10-33, pH=9.3ʱ��Mg2+��ʼ����]��
(4����μ�����Һ��Fe3+�Ƿ������������������__________��
(5��ƫ���ᰱ����VOSO4��Һ�м�������ؽ���������Ȼ���ð�ˮ����pH�����Ƶã�д��VO2+����������������ӷ���ʽ_________��
(6������a t��������Mg(VO3)2�����������̵IJ���Ϊ6%������������Mg(VO3)2��Ʒ��
����Ϊ_________t ���ú�a��b�Ĵ���ʽ��ʾ����
���𰸡� +5 ![]() ˮԡ���� Mg2+��Fe2+��Fe3+��Al3+ ���ά 2Fe2++H2O2+2H+=2Fe3++H2O 5<pH<9.3 ȡ������Һ���Թ��У������еμ������軯����Һ�������Һ�����ɫ��˵����Һ�в���Fe3+��Fe3+�������������Һ���ɫ��˵����Һ�к�Fe3+, Fe3+δ������ 6VO2-+ ClO3-+9H2O=Cl-+6VO3-+18H+
ˮԡ���� Mg2+��Fe2+��Fe3+��Al3+ ���ά 2Fe2++H2O2+2H+=2Fe3++H2O 5<pH<9.3 ȡ������Һ���Թ��У������еμ������軯����Һ�������Һ�����ɫ��˵����Һ�в���Fe3+��Fe3+�������������Һ���ɫ��˵����Һ�к�Fe3+, Fe3+δ������ 6VO2-+ ClO3-+9H2O=Cl-+6VO3-+18H+ ![]()
����������������� (l) ���ݻ��ϼ۴����͵���0����Mg(VO3)2 ��V�Ļ��ϼ���ƫ��������Ȼ�þ��Ӧ���ɸ��������Ȼ����
(2��һ����ˮԡ���ȵķ���ȷ���Ʒ�Ӧ�¶ȡ�SiO2�������Ӧ�� MgO��Fe2O3��FeO��Al2O3�ֱ������ᷴӦ�����Ȼ�þ���Ȼ������Ȼ��������Ȼ���������1��SiO2��
(3)����˫��ˮ����Fe2+����ΪFe3+���������������ܽ�ȴ�����������������Ksp[Al(OH)3]=1��10-33����Al3+Ũ�Ⱦ�С��l��10-6mol��L-1ʱOH-Ũ�����ж�PH��Сֵ��Ϊ��ֹMg2+����������PH�����ֵΪ9.3��
(4��Fe3+�����軯����Һ��Ӧ����Һ���ɫ��
(5��VO2+�����������ΪVO3-�����ݵ�ʧ�����غ�ƽ�ⷽ��ʽ��
(6������þԪ���غ������������Mg(VO3)2��Ʒ��������
�������������Ϸ�����(l) Mg(VO3)2 ��V�Ļ��ϼ�+5��ƫ��������Ȼ�þ��Ӧ���ɸ��������Ȼ�泥��Ȼ�������ӻ��������ʽΪ![]() ��
��
(2����ˮԡ���ȵķ���ȷ���Ʒ�Ӧ�¶�Ϊ80�档SiO2�������Ӧ�� MgO��Fe2O3��FeO��Al2O3�ֱ������ᷴӦ�����Ȼ�þ���Ȼ������Ȼ��������Ȼ�������Һ�е���������Mg2+��Fe2+��Fe3+��Al3+������1��SiO2��������������ά��
(3)����˫��ˮ����Fe2+����ΪFe3+�����ӷ���ʽΪ2Fe2++H2O2+2H+=2Fe3++H2O���������������ܽ�ȴ�����������������Ksp[Al(OH)3]=1��10-33��Al3+Ũ�Ⱦ�С��l��10-6mol��L-1ʱc(OH-)>![]() , PH��Сֵ5��Ϊ��ֹMg2+����������PH�����ֵΪ9.3������PH�ķ�Χ��5<pH<9.3��
, PH��Сֵ5��Ϊ��ֹMg2+����������PH�����ֵΪ9.3������PH�ķ�Χ��5<pH<9.3��
(4��ȡ������Һ���Թ��У������еμ������軯����Һ�������Һ�����ɫ��˵����Һ�в���Fe3+��Fe3+�������������Һ���ɫ��˵����Һ�к�Fe3+, Fe3+δ��������
(5��VO2+�����������ΪVO3-�����ӷ���ʽΪ6VO2-+ ClO3-+9H2O=Cl-+6VO3-+18H+��
(6������������Mg(VO3)2��Ʒ������Ϊxt
MgO ~~~~~~ Mg(VO3)2��52.1%
40 222
a��52.1%��b% x
![]() ��x=
��x=![]() ��
��

����Ŀ��������Ʒ����Ч�ɷּ���;��Ӧ�������
ѡ�� | A | B | C | D |
��Ʒ | ʳ�� | С�մ� | ������������Ƭ | Ư�� |
��Ч�ɷ� | NaCl | Na2CO3 | Al(OH)3 | Ca(ClO)2 |
��; | ����ζƷ | �����ͷ� | ������ҩ | �������� |
A. A B. B C. C D. D