题目内容
1.已知: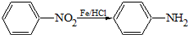 (苯胺,易被氧化).甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物.以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下.
(苯胺,易被氧化).甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物.以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下.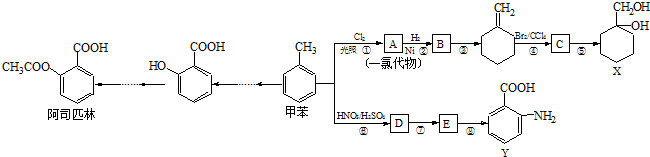
请回答下列问题:
(1)甲苯的1H核磁共振谱图中有4个特征峰.
(2)中间产物D与目标产物Y的关系是同分异构体.
(3)写出结构简式:A
 ,C
,C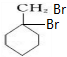 ,E
,E .
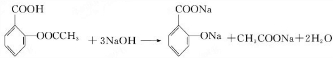
.(4)写出阿司匹林与足量的NaOH(aq)反应的化学方程式:
 .
.
分析 甲苯分子中有4种化学环境不同的氢原子,甲苯的1H核磁共振谱图中有4个特征峰. 与氯气在光照条件下甲基中H原子被取代生成一氯代物A,则A为
与氯气在光照条件下甲基中H原子被取代生成一氯代物A,则A为 ,A与氢气发生加成反应生成B为
,A与氢气发生加成反应生成B为 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,
, 与溴发生加成反应生成C为
与溴发生加成反应生成C为 ,C在氢氧化钠水溶液、加热条件下发生水解反应生成X.
,C在氢氧化钠水溶液、加热条件下发生水解反应生成X. 在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应Y的结构可知D为
在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应Y的结构可知D为 ,D转化生成E,由于苯胺容易被氧化,D中甲基在酸性高锰酸钾条件下被氧化物-COOH,故E为
,D转化生成E,由于苯胺容易被氧化,D中甲基在酸性高锰酸钾条件下被氧化物-COOH,故E为 ,E发生还原反应硝基被还原为氨基生成Y,据此解答.
,E发生还原反应硝基被还原为氨基生成Y,据此解答.
解答 解:甲苯分子中有4种化学环境不同的氢原子,甲苯的1H核磁共振谱图中有4个特征峰. 与氯气在光照条件下甲基中H原子被取代生成一氯代物A,则A为
与氯气在光照条件下甲基中H原子被取代生成一氯代物A,则A为 ,A与氢气发生加成反应生成B为
,A与氢气发生加成反应生成B为 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成 ,
, 与溴发生加成反应生成C为
与溴发生加成反应生成C为 ,C在氢氧化钠水溶液、加热条件下发生水解反应生成X.
,C在氢氧化钠水溶液、加热条件下发生水解反应生成X. 在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应Y的结构可知D为
在浓硫酸、加热条件下与浓硝酸发生取代反应生成F,结合反应Y的结构可知D为 ,D转化生成E,由于苯胺容易被氧化,D中甲基在酸性高锰酸钾条件下被氧化物-COOH,故E为
,D转化生成E,由于苯胺容易被氧化,D中甲基在酸性高锰酸钾条件下被氧化物-COOH,故E为 ,E发生还原反应硝基被还原为氨基生成Y;
,E发生还原反应硝基被还原为氨基生成Y;
(1) 中含有4种氢原子,所以核磁共振氢谱有4个吸收峰,故答案为:4;
中含有4种氢原子,所以核磁共振氢谱有4个吸收峰,故答案为:4;
(2)二者分子式相同结构不同,所以属于同分异构体,故答案为:同分异构体;
(3)通过以上分析知,A为 ,C为
,C为 ,E为
,E为 ,
,
故答案为: ;
; ;
; ;
;
(4)由阿司匹林结构可知,1mol阿司匹林含有1mol-COOH、1mol酯基,该酯基是酸与酚形成的,1mol该酯基能与2molNaOH反应,1mol-COOH与1mol NaOH反应,故1mol阿司匹林最多消耗3mol NaOH,故阿司匹林与足量的NaOH(aq)反应的化学方程式为: ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,明确官能团及其性质关系、物质之间的转化是解本题关键,根据某些物质的结构简式结合反应条件进行推断,注意阿司匹林水解生成的酚羟基能和NaOH反应,题目难度不大.

| A. | 200mL 1mol/L的NaCl溶液 | B. | 150 mL 1mol/L的MgCl2溶液 | ||
| C. | 100mL 1mol/L的HCl溶液 | D. | 50mL 1mol/L的AlCl3溶液 |
【查阅资料】25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
【实验探究】向2支均盛有1mL0.1mol/L的MgCl2溶液中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀;(1)分别向两支试管中加入不同试剂,记录实验现象如表:
| 实验编号 | 加入试剂 | 实验现象 |
| Ⅰ | 2滴 0.1mol/L FeCl3 溶液 | ①白色沉淀转化为红褐色沉淀 |
| Ⅱ | 4mL2mol/LNH4Cl溶液 | ②白色沉淀溶解,得无色溶液 |
(3)同学们猜想实验Ⅱ中沉淀溶解的原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动.
猜想2:NH4Cl水解出来的H+与Mg(OH)2电离出OH-结合成水,使Mg(OH)2的溶解平衡正向移动.
(4)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解.
①实验证明猜想正确的是1(填“1“或“2“).
②验证猜想时,设计实验向氢氧化镁沉淀中加NH4Cl和氨水混合液的理由是做对比分析,pH=8的NH4Cl和氨水混合液中c(H+)很小,可以否定猜想2.
| A. | CO2为V形的极性分子 | |
| B. | SO2与O3互为等电子体 | |
| C. | NaCl的晶格能高于KCl | |
| D. | 第一电离能由高到低的顺序为:F>O>N |
| A. | CH3CH2OH+CH3COOH $?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O | |
| B. | CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O | |
| C. | 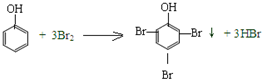 | |
| D. | CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O |
 ;NH3的稳定性比PH3的强(填“强”或“弱”).
;NH3的稳定性比PH3的强(填“强”或“弱”).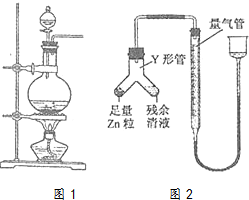 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示)
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示)