题目内容
某反应X+3Y=2Z+2P在甲、乙、丙、丁四种不同条件下测得的反应速率为:
甲:vx=0.3mol/L.min 乙:vy=1.2mol/L.min 丙:vz=0.8mol/L.min 丁:vp=0.9mol/L.min 则反应进行最快的是( )
甲:vx=0.3mol/L.min 乙:vy=1.2mol/L.min 丙:vz=0.8mol/L.min 丁:vp=0.9mol/L.min 则反应进行最快的是( )
| A、甲 | B、乙 | C、丙 | D、丁 |
考点:化学反应速率和化学计量数的关系
专题:化学反应速率专题
分析:由于不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意应单位一致.
解答:
解:由于不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,
甲:
=0.3mol/(L.min ),乙:
=0.4mol/(L.min),丙:
=0.4mol/(L.min),丁:
=0.45mol/(L.min ),故反应速率:丁>乙=丙>甲,
故选D.
甲:
| vx |
| 1 |
| vy |
| 3 |
| vz |
| 2 |
| vp |
| 2 |
故选D.
点评:本题考查化学反应速率快慢比较,难度不大,利用比值法可以迅速判断,也可以转化为同一物质表示的速率再进行比较.

练习册系列答案
相关题目
浓度为2mol?L-1的NaOH溶液150mL,吸收了4.48LCO2(标准状况).下列说法正确的是( )
| A、HCO3-离子数略多于CO32-离子数 |
| B、HCO3-离子数等于CO32-离子数 |
| C、HCO3-离子数略少于CO32-离子数 |
| D、Na+离子数等于HCO3-离子数和CO32-离子数之和 |
将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol/LNaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是( )
| A、加入合金的质量可能为9.6g |
| B、参加反应的硝酸的物质的量为0.4mol |
| C、沉淀完全时消耗NaOH溶液体积为150mL |
| D、溶解合金时产生NO气体体积2.24L(STP) |
在容积为1L的干燥烧瓶中,用向下排空气法充入NH3后,测得烧瓶中的气体对氢气的相对密度为9.7.若将此气体进行喷泉实验,当喷泉停止后进入烧瓶中溶液的体积应为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
有一铁粉和氧化铜的混合物6.96g,进行如下实验:
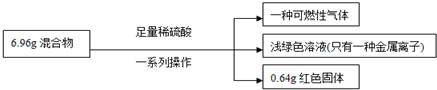
根据实验所得数据,关于混合物相关说法正确的是( )

根据实验所得数据,关于混合物相关说法正确的是( )
| A、原混合物中铁的质量分数无法计算 |
| B、实验中反应的H2SO4 用浓稀均可 |
| C、生成气体质量为0.2g |
| D、原混合物中铜元素的质量不一定为0.64g |
以KCl和ZnCl2混合液为电镀液在铁制品上镀锌,下列说法正确的是( )
| A、镀锌层破损后即对铁制品失去保护作用 |
| B、未通电前上述电镀装置可构成原电池,电镀过程是该原电池的充电过程 |
| C、电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D、因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |