题目内容
已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
| A、H20(g)═H2 (g)+l/202(g)△H=+242kJ.mol-l | ||
| B、2H2 (g)+02 (g)═2H20(1)△H=-484kJ.mol-l | ||
C、H2(g)+
| ||
| D、2H2(g)+02( g)═2 H2 0(g)△H=-242kJ.mol-1 |
考点:热化学方程式
专题:化学反应中的能量变化
分析:A、根据氢气燃烧生成水蒸气的逆过程为吸热过程来分析;
B、根据物质的聚集状态来判断;
C、根据反应放热时焓变符号为负来判断;
D、根据反应热与氢气的量之间的对应关系来判断.
B、根据物质的聚集状态来判断;
C、根据反应放热时焓变符号为负来判断;
D、根据反应热与氢气的量之间的对应关系来判断.
解答:
解:A、2mol氢气燃烧生成水蒸气放出484kJ热量,则1mol氢气燃烧生成水蒸气放出242kJ热量,其逆过程就要吸收这些热量,有:H2O(g)=H2(g)+
O2(g)△H=+242kJ?mol-1,故A正确;
B、生成的水应该为气态,而不是液态,故B错误;
C、反应为放热反应,此时焓变符号为负,故C错误;
D、2mol氢气燃烧生成水蒸气放出484kJ,反应热的数值错误,故D错误.
故选A.
| 1 |
| 2 |
B、生成的水应该为气态,而不是液态,故B错误;
C、反应为放热反应,此时焓变符号为负,故C错误;
D、2mol氢气燃烧生成水蒸气放出484kJ,反应热的数值错误,故D错误.
故选A.
点评:本题主要考查学生热化学方程式的书写原则,该题型是现在高考的热点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
海水是一个巨大的化学资库,下列有关海水综合利用的说法正确的是( )
| A、从海水中可得到NaCl,电解熔融NaCl或其水溶液都可制得Cl2 |
| B、因海水中含有镁元素,故不需经过化学变化就可以得到镁单质 |
| C、利用蒸馏原理从海水中提取淡水是海水淡化技术发展的新方向 |
| D、无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能 |
能说明醋酸是弱电解质的事实是( )
| A、醋酸水溶液能使湿润的蓝色石蕊试纸变红 |
| B、醋酸和碳酸钠溶液反应放出二氧化碳 |
| C、c(H+)相同的醋酸和盐酸相比较,醋酸溶液的浓度大 |
| D、浓度和体积均相同的醋酸和盐酸可中和等物质的量的NaOH |
炼铁的总反应为 Fe2O3(s)+3CO(g)→2Fe(s)+3CO2(g)+Q kJ,可能发生了以下过程:
3Fe2O3(s)+CO(g)→2Fe3O4(s)+CO2(g)+Q1 kJ;
Fe3O4(s)+CO(g)→3FeO(s)+CO2(g)+Q2 kJ;
FeO(s)+CO(g)→Fe(s)+CO2(g)+Q3 kJ.
则Q与Q1、Q2、Q2的关系式正确的是( )
3Fe2O3(s)+CO(g)→2Fe3O4(s)+CO2(g)+Q1 kJ;
Fe3O4(s)+CO(g)→3FeO(s)+CO2(g)+Q2 kJ;
FeO(s)+CO(g)→Fe(s)+CO2(g)+Q3 kJ.
则Q与Q1、Q2、Q2的关系式正确的是( )
| A、Q=Q1+Q2+Q3 | ||
| B、Q=Q1-Q2-Q3 | ||
C、Q=
| ||
D、Q=
|
海底有大量的天然气水合物,可满足人类1000年的能源需要.天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子.若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为( )
| A、CH4?14H2O | ||
| B、CH4?8H2O | ||
C、CH4?
| ||
| D、CH4?6H2O |
同温同压下,气体的密度之比等于相对分子质量之比,已知空气的平均相对分子质量为29,同温同压下,下列气体的密度比空气密度小的是( )
| A、二氧化氮 | B、二氧化碳 |
| C、二氧化硫 | D、一氧化碳 |
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | -1 | +1 | -4 | -2 |
| A、丙的常见氧化物有两种 |
| B、气态氢化物稳定性:丁>戊 |
| C、丁的氧化物能与乙的氢化物的水溶液反应 |
| D、原子半径大小:丙<丁 |
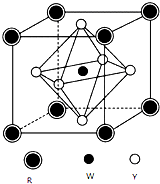 前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题:
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题: