题目内容
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲、乙、丙、丁、戊的化合价如下,下列说法正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 化合价 | -4 | -1 | +1 | -4 | -2 |
| A、丙的常见氧化物有两种 |
| B、气态氢化物稳定性:丁>戊 |
| C、丁的氧化物能与乙的氢化物的水溶液反应 |
| D、原子半径大小:丙<丁 |
考点:原子结构与元素的性质
专题:
分析:已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲为-4价,乙为-1价,丙为+1加,丁为-4价,戊为-2价,则甲为C元素,乙为F元素,丙为Na元素,丁为Si元素,戊为S元素,结合各元素化合物的性质分析.
解答:
解:已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,其氢化物中甲为-4价,乙为-1价,丙为+1加,丁为-4价,戊为-2价,则甲为C元素,乙为F元素,丙为Na元素,丁为Si元素,戊为S元素,
A.丙为Na元素,其氧化物有氧化钠和过氧化钠两种,故A正确;
B.非金属性越强,其氢化物的稳定性越强,丁为Si元素,戊为S元素,非金属性:Si<S,则气态氢化物稳定性:丁<戊,故B错误;
C.丁的氧化物为SiO2,乙的氢化物为HF,则二者反应SiO2+4HF=SiF4↑+H2O,故C正确;
D.同周期从左到右原子半径逐渐减小,丙为Na元素,丁为Si元素,则原子半径大小:Na>Si,即丙>丁,故D错误;
故选AC.
A.丙为Na元素,其氧化物有氧化钠和过氧化钠两种,故A正确;
B.非金属性越强,其氢化物的稳定性越强,丁为Si元素,戊为S元素,非金属性:Si<S,则气态氢化物稳定性:丁<戊,故B错误;
C.丁的氧化物为SiO2,乙的氢化物为HF,则二者反应SiO2+4HF=SiF4↑+H2O,故C正确;
D.同周期从左到右原子半径逐渐减小,丙为Na元素,丁为Si元素,则原子半径大小:Na>Si,即丙>丁,故D错误;
故选AC.
点评:本题考查元素周期律及元素对应的单质、化合物的性质,元素的推断是解答本题的关键,注意根据氢化物中元素的化合价以及原子序数的关系分析推断元素,难度不大.

练习册系列答案
相关题目
已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
| A、H20(g)═H2 (g)+l/202(g)△H=+242kJ.mol-l | ||
| B、2H2 (g)+02 (g)═2H20(1)△H=-484kJ.mol-l | ||
C、H2(g)+
| ||
| D、2H2(g)+02( g)═2 H2 0(g)△H=-242kJ.mol-1 |
取19.2g铜跟少量的浓硝酸反应,铜全部溶解后,收集到NO2、NO混合气体的体积11.2L(标准状况),反应消耗硝酸的物质的量是( )
| A、0.5mol |
| B、0.8mol |
| C、1.1mol |
| D、1.2mol |
下列说法不正确的是( )
| A、在稀氨水中滴加AgNO3溶液来配制银氨溶液,银氨溶液久置容易爆炸,要随配随用 |
| B、用标准NaOH溶液测定食醋中醋酸含量时应该使用酚酞作为指示剂 |
| C、将饱和氯水滴到淀粉碘化钾试纸上,如果试纸先变蓝后变白,说明氯水具有强氧化性 |
| D、重结晶法提纯KNO3产品除去少量NaCl时,应在较高温度下溶解产品配成浓溶液后冷却结晶 |
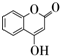 是一种医药中间体,常用来制备抗凝血药,可通过如图路线合成
是一种医药中间体,常用来制备抗凝血药,可通过如图路线合成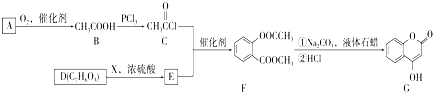
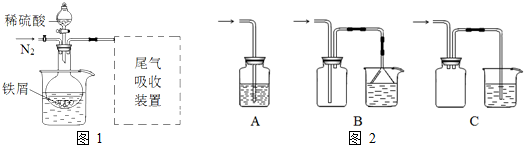
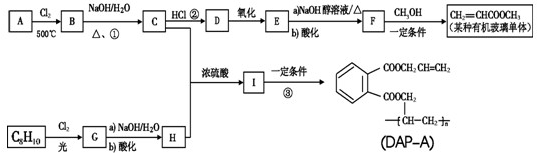
 硫代硫酸钠(Na2S2O3)是常用的还原剂.在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C被完全氧化,剩余的I2用Na2S2O3标准溶液滴定,可测定溶液中维生素C的含量.发生的反应为:C6H8O6+I2═C6H6O6+2H++2I-2S2O32-+I2═S4O62-+2I-
硫代硫酸钠(Na2S2O3)是常用的还原剂.在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C被完全氧化,剩余的I2用Na2S2O3标准溶液滴定,可测定溶液中维生素C的含量.发生的反应为:C6H8O6+I2═C6H6O6+2H++2I-2S2O32-+I2═S4O62-+2I-