题目内容
6. 短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )| A. | X、Y、Z元素的离子半径大小是X>Y>Z | |
| B. | X元素的氢化物沸点比同主族元素的氢化物低 | |
| C. | Q形成的单质在化学反应中只体现氧化性 | |
| D. | Q的氧化物对应水化物的酸性在同主族元素中是最强的 |
分析 短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,0.1mol•L-1D溶液的pH为1,D为HCl,D是由W与Q形成的化合物,W为H,Q为Cl;B是两性氢氧化物,则B为Al(OH)3,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性,A为NaAlO2;结合转化可知C为AlCl3,再结合原子序数可知,X为O,Y为Na,Z为Al,以此解答该题.
解答 解:由上述分析可知,W为H,X为O,Y为Na,Z为Al,Q为Cl,
A.具有相同电子排布的离子中,原子序数大的离子半径小,则X、Y、Z元素的离子半径大小是X>Y>Z,故A正确;
B.水分子间含氢键,则X元素的氢化物沸点比同主族元素的氢化物高,故B错误;
C.氯气与水的反应中,只有Cl元素化合价发生变化,则氯气既是氧化剂也是还原剂,既表现氧化性也表现还原性,故C错误;
D.Q的最高价氧化物对应的水化物为高氯酸,酸性最强,如不是最高价,则酸性强弱不能确定,故D错误;
故选A.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应、元素周期律等为解答的关键,侧重分析与推断能力的考查,注意两性化合物为推断的突破口,题目难度不大.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
2.四种短周期主族元素W、X、Y、Z、M的原子序数依次增大,W的原子中只有1个电子,X2-和Y+离子的电子层结构相同,Z与X同族,M与Y形成的离子化合物的水溶液呈中性.下列叙述错误的是( )
| A. | W与其他四种元素形成的二元化合物中其化合价均为+1 | |
| B. | X与Y形成的化合物溶于水后溶液呈碱性 | |
| C. | 最高价氧化物的水化物的酸性:M>Z | |
| D. | 简单离子半径:W<Y<X<Z |
17.化学是你,化学是我,化学深入我们生活,下列说法正确的是( )
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 煤是混合物,含有大量的芳香烃 |
14.LiFePO4新型锂离子动力电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.已知该电池放电时的电极反应式为:正极:FePO4+Li++e-═LiFePO4,负极:Li-e-═Li+.下列说法正确的是( )
| A. | 充电时电池反应式为FePO4+Li═LiFePO4 | |
| B. | 放电时在正极上是Li+得电子被还原 | |
| C. | 放电时电池内部Li+向正极移动 | |
| D. | 充电时动力电池上“+”的电极与外接电源的负极相连 |
11. 短周期元素X、Y、Z.W的原子序数依次增大.在如图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物.常温时,0.1mol•L-1的a溶液的pH为1,d为红棕色气体,e为无色气体.下列说法正确的是( )
短周期元素X、Y、Z.W的原子序数依次增大.在如图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物.常温时,0.1mol•L-1的a溶液的pH为1,d为红棕色气体,e为无色气体.下列说法正确的是( )
 短周期元素X、Y、Z.W的原子序数依次增大.在如图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物.常温时,0.1mol•L-1的a溶液的pH为1,d为红棕色气体,e为无色气体.下列说法正确的是( )
短周期元素X、Y、Z.W的原子序数依次增大.在如图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物.常温时,0.1mol•L-1的a溶液的pH为1,d为红棕色气体,e为无色气体.下列说法正确的是( )| A. | 元素的非金属性:Y>Z>X | |
| B. | 反应①中消耗lmola时转移电子数与反应②中生成1mol a时转移电子数相等 | |
| C. | 原子半径的大小:y<Z<W | |
| D. | Y的氢化物常温常压下为气态 |
15.目前国际空间站处理CO2废气涉及的反应为CO2+4H2$\stackrel{钌催化剂}{?}$CH4+2H2O.关于该反应的下列说法正确的是( )
| A. | 钌催化剂能加快该反应的速率 | B. | 升高温度能减慢该反应的速率 | ||
| C. | 达到平衡时,CO2能100%转化为CH4 | D. | 达到平衡时,反应速率:v(正)=v(逆)≠0 |
18.某温度下,反应N2O4(g)?2NO2(g)(△H>0)在密闭容器中达到平衡.下列说法不正确的是( )

| A. | 加压时(体积变小),平衡向逆反应方向移动,将使正反应速率增大 | |
| B. | 某时刻改变条件速率时间如图,改变的条件是恒容时增大N2O4的浓度 | |
| C. | 保持体积不变,加入少许N2O4,平衡向正反应方向移动,再达平衡时颜色变深 | |
| D. | 保持压强不变,加入少许N2O4,混合气体的相对平均分子质量不变 |
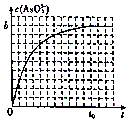 砷(As)是第四周期第VA族的元素,能形成多种化合物.回答下列问题:
砷(As)是第四周期第VA族的元素,能形成多种化合物.回答下列问题: .
.