题目内容
3.如图所示的四个容器中分别盛有不同的溶液,除a、b外,其余电极均为石墨电极.甲为铅蓄电池,其工作原理为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb.闭合K,发现g电极附近的溶液先变红,20min后,将K断开,此时c、d两极上产生的气体体积相同;据此回答: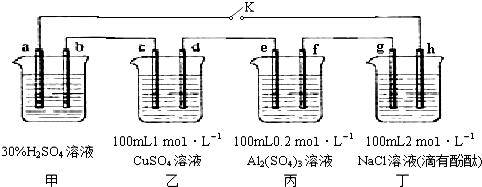
(1)a电极的电极材料是PbO2(填“PbO2”或“Pb”).
(2)丙装置中发生电解的总反应方程式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑.
(3)电解20min时,停止电解,此时要使乙中溶液恢复到原来的状态,需要加入的物质是Cu(OH)2,其物质的量是0.01mol
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连接上灵敏电流计,发现电流计指针偏转,则此时c电极为负极,d电极上发生反应的电极反应式为O2+4H++4e-=2H2O.
(5)电解后,丁装置中两电极共收集到0.35mol气体.
分析 甲池是原电池做电源,发生的反应为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O;乙丙丁是电解池,闭合K,发现g电极附近的溶液变红,说明g电极是电解池的阴极,h是电解池的阳极;所以a为正极,b为负极;c电极为阴极,d为阳极;e电极为阴极,f为阳极;20min后,将K断开,此时c、d两极上产生的气体体积相同,
(1)依据分析判断电极名称;
(2)丙中电解水;
(3)c、d两极上产生的气体体积相同,c电极上发生的电极反应为:Cu2++2e-=Cu;2H++2e-=H2↑,d电极上发生的电极反应为:4OH--4e-=2H2O+O2↑,根据电子守恒计算生成的Cu、氢气和氧气的物质的量;
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连上灵敏电流计,发现电流计指针偏转,说明形成了原电池反应,氢气在c极失电子,氧气在d极得电子;
(5)d极生成0.1mol氧气,转移0.4mol电子,丁装置中含有0.2molNaCl,阳极分别发生2Cl--2e-=Cl2↑、4OH--4e-=2H2O+O2↑,阴极发生2H++2e-=H2↑,结合电极方程式计算.
解答 解:甲池是原电池做电源,发生的反应为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O;乙丙丁是电解池,闭合K,发现G电极附近的溶液变红,说明G电极是电解池的阴极,H是电解池的阳极;所以a为正极,b为负极;c电极为阴极,d为阳极;e电极为阴极,f为阳极;20min后,将K断开,此时c、d两极上产生的气体体积相同,
(1)a电极是铅蓄电池的正极,正极的电极材料是PbO2;
故答案为:PbO2;
(2)丙中电解硫酸铝,其实际上是电解水,其电解方程式为:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑;
故答案为:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑;
(3)c、d两极上产生的气体体积相同,c电极上发生的电极反应为:Cu2++2e-=Cu;2H++2e-=H2↑,d电极上发生的电极反应为:4OH--4e-=2H2O+O2↑,
设生成的氧气为xmol,则氢气也为xmol,生成的Cu为0.1L×1mol/L=0.1mol,由得失电子可得:2x+0.1×2=4x,解得x=0.1mol,
则电解时生成0.1mol氢气、0.1mol氧气和0.1molCu,若要恢复到原来的状态,需要加入0.1molCu(OH)2;
故答案为:Cu(OH)2;0.1mol;
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连上灵敏电流计,发现电流计指针偏转,说明形成了原电池反应,氢气在c极失电子,c为负极,氧气在d极得电子,正极的反应为:O2+4H++4e-=2H2O;
故答案为:负;O2+4H++4e-=2H2O;
(5)d极生成0.1mol氧气,转移0.4mol电子,丁装置中含有0.2molNaCl,阳极分别发生2Cl--2e-=Cl2↑、4OH--4e-=2H2O+O2↑,阴极发生2H++2e-=H2↑,则阳极上先生成0.1mol氯气,再生成0.05mol氧气,阴极生成0.2mol氢气,共生成0.35mol气体,故答案为:0.35.
点评 本题考查了原电池和电解池原理在计算中的应用等,正确判断原电池正负极和电解池的阴阳极、以及电极方程式的书写方法是解本题关键,根据离子放电顺序确定阴阳极电极反应,并结合得失电子守恒解答,难度中等.

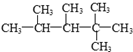 是由一种单烯烃加氢而成的,那么原烯烃的可能结构有( )
是由一种单烯烃加氢而成的,那么原烯烃的可能结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
| A. | 1 mol乙炔分子所含的共用电子对总数为5NA | |
| B. | 1 mol甲基(-CH3 )所含的电子总数为9NA | |
| C. | 0.5 mol 1,3-丁二烯分子中含有碳碳双键总数为NA | |
| D. | 标准状况下,22.4L己烷完全燃烧所生成的气态产物的分子数为7NA |
| A. | NO3- K+[Al(OH)4]- OH- | B. | Na+ Ba2+ Mg2+ HCO3- | ||
| C. | NO3- Mg2+ K+ Cl- | D. | NH4+ NO3- CO32- Na+ |
①加热试管时,先均匀加热,后局部加热
②做H2还原CuO实验时,先通H2,后加热CuO,反应完毕后,先撤酒精灯待试管冷却,后停止通H2
③制取气体时,先检查装置气密性,后装药品
④点燃可燃性气体如H2、CO等时,先检验气体纯度,后点燃
⑤制取蒸馏水时,先通冷却水,后加热烧瓶
⑥进行分液操作时,先从上口倒出上层液体,后从通过下端活塞放出下层液体.
| A. | ①②③④ | B. | ①②③④⑤ | C. | ①②③④⑥ | D. | 全部 |
| A. | 二氧化硫具有还原性,可用二氧化硫水溶液吸收溴蒸气 | |
| B. | 氢氟酸具有强酸性,可用氢氟酸蚀刻玻璃 | |
| C. | 氨气具有氧化性,可用浓氨水检验氯气管道是否泄漏 | |
| D. | SiO2的导电能力强,可用于制造通讯光缆 |
| A. | 在复盐NH4Fe(SO4)2溶液中加入过量的Ba(OH)2溶液:NH4++Fe3++2SO42-+2Ba2++4OH-═2BaSO4↓+Fe(OH)3↓+NH3•H2O | |
| B. | 在盐碱地(含较多NaCl、Na2CO3)上通过施加适量CaSO4可降低土壤的碱性:CaSO4+Na2CO3═CaCO3+Na2SO4 | |
| C. | 在燃煤时加入适量石灰石粉末,可减少SO2的排放:CaCO3+SO2═CaSO3+CO2 | |
| D. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2H++2I-+H2O2═I2+2H2O |
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化.
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色
Ⅲ.向Ⅱ中所得的溶液中加入BaCl2溶液,有白色沉淀生成
Ⅳ.向Ⅱ所得的溶液中加入过量浓氨水,仅有红褐色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成.
请回答下列问题:
(1)该废水一定含有的离子是Fe2+、Cu2+、NO3-、SO42-,可能含有的离子是Cl-;
(2)实验Ⅱ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(3)过滤除去Ⅳ中的蓝色沉淀,调整滤液的pH为10.7左右时,加入铝粉,产生氨气和氮气的体积比为1:4,其离子方程式为:Al+NO3-+OH-→AlO2-+NH3+N2+H2O(未配平),还原产物是NH3和NO;
(4)工业废水中常含有不同类型的污染物,可采用不同的方法处理,下列处理措施和方法中正确的是AD.
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 碱性的废水 | 用CO2中和 | 化学法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 废酸 | 加生石灰中和 | 化学法 |
| A. | O2 | B. | SO2 | C. | KCl | D. | KOH |