题目内容
2.在标准状况下,与12g H2的体积相等的N2( )| A. | 质量为12g | B. | 物质的量为6mol | ||
| C. | 体积约为22.4L | D. | 分子数约为6.02×1023 |
分析 根据n=$\frac{m}{M}$计算氢气物质的量,标况下氮气与氢气体积相等,而二者物质的量相等,根据m=nM计算氮气质量、根据V=nVm计算氮气体积,根据N=nNA计算氮气分子数目.
解答 解:12g H2的物质的量为$\frac{12g}{2g/mol}$=6mol,标况下氮气与氢气体积相等,则氮气物质的量为6mol,则氮气质量为6mol×28g/mol=168g,标况下氮气体积为6mol×22.4L/mol=134.4L,氮气分子数目为6×6.02×1023,故B正确,ACD错误,故选:B.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心计算,有利于基础知识的巩固.

练习册系列答案
相关题目
12.下列事故处理方法正确的是( )
| A. | 汽油失火时,立即用水灭火 | |
| B. | 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 | |
| C. | 浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 | |
| D. | 实验室不小心碰翻酒精灯引起实验桌上洒落的少量酒精起火时,迅速用泡沫灭火器灭火 |
13.下列有关化学用语描述正确的是( )
| A. | 乙醇的分子式C2H5OH | B. | 硫离子的结构示意图: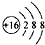 | ||
| C. | NH4Cl的电子式: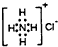 | D. | 对氯甲苯的结构简式: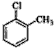 |
10.下列溶液中,与100mL 0.5mol/L NaCl溶液所含的Cl-的物质的量相同的是( )
| A. | 200 mL 0.25 mol/L CaCl2溶液 | B. | 100 mL 0.25 mol/L HCl溶液 | ||
| C. | 50 mL 1mol/L NaCl溶液 | D. | 100 mL 0.5 mol/L MgCl2 溶液 |
14.某强氧化剂XO(OH)2+能被Na2SO3还原到较低价态.如果还原含2.4×10-3mol XO(OH)2+的溶液至较低价态,需要30mL 0.2mol/L 的Na2SO3溶液,那么X元素的最终价态是( )
| A. | +2 | B. | +1 | C. | 0 | D. | -1 |
11.下列说法错误的是( )
| A. | 石油的炼制过程不都是化学变化 | |
| B. | 煤中含有苯和甲苯,可用蒸馏的方法将它们分离 | |
| C. | 煤是工业上获得芳香烃的一种重要原料 | |
| D. | 煤通过液化和气化处理能减少环境污染 |
12.下列说法不正确的是( )
| A. | 绿色化学的核心就是利用化学原理减少和消除工业生产对环境的污染 | |
| B. | 石油是由多种碳氢化合物组成的混合物 | |
| C. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 | |
| D. | 煤的干馏是将煤隔绝空气加强热使之分解的过程 |