题目内容
8.下列各装置图的叙述中,错误的是( )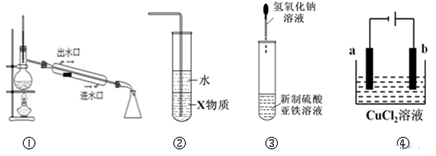
| A. | 实验室用装置①蒸馏石油 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③可用于制备氢氧化亚铁并观察其颜色 | |
| D. | 装置④是电解精炼铜,b极为粗铜,发生氧化反应 |
分析 A.根据温度计位置、冷凝管通水方向等方面判断;
B.四氯化碳的密度大于水,且氨气不溶于四氯化碳,可以利用该装置吸收氨气;
C.氢氧化亚铁易被氧化,应该将胶头滴管下端插入硫酸亚铁溶液中;
D.电解精炼铜时,粗铜与阳极相连、纯铜与引进相连.
解答 解:A.装置①为蒸馏装置,该装置中温度计位置、冷凝管的通水方向等都合理,能够达到实验目的,故A不选;
B.氨气极易溶于水,吸收氨气时需要防止倒吸,若装置②中X若为四氯化碳,氨气不溶于四氯化碳,可用该装置吸收氨气,并防止倒吸,故B不选;
C.氢氧化亚铁易被空气中氧气氧化,应将胶头滴管下端插入硫酸亚铁溶液中或用苯隔绝空气,故C选;
D.根据图示可知,a为阴极、b为阴极,电解精炼铜,b极(阳极)为粗铜,粗铜失去电子生成铜离子,发生氧化反应,故D不选;
故选C.
点评 本题考查化学实验方案的评价,题目难度不大,涉及氨气的制备、氢氧化亚铁的制备以及原电池知识,明确常见化学实验基本操作方法为解答关键,试题侧重于考查学生化学实验方案的评价能力和实验操作能力,注意把握实验原理和实验注意事项.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
18.无放射性的同位素被称之为“稳定同位素”,在陆地生态系统研究中,2H、13C、15N、18O、34S等常作环境分析指示物.下列有关一些“稳定同位素”的说法错误的是( )
| A. | 34S原子核内中子数为18 | B. | 2H+的酸性比1H+的酸性更强 | ||
| C. | 16O与18O的化学性质几乎完全相同 | D. | 13C和15N原子核内的质子数相差1 |
19. 将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )
将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )
 将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )
将高科技用于现代军事备受关注.用于制造隐形飞机的物质A 具有吸收微波的功能,其主要成分的结构如图,关于该物质的说法正确的是( )| A. | 该物质属于无机物 | |
| B. | 该物质是一种芳香烃 | |
| C. | 该物质不可能使溴水褪色 | |
| D. | 1mol该物质最多可与3molH2发生加成反应 |
16.下列有关原电池的说法中不正确的是( )
| A. | 在内电路中,电子由正极流向负极 | |
| B. | 原电池的正、负极材料不一定都参与反应 | |
| C. | 原电池工作时,正极上发生还原反应 | |
| D. | 原电池工作时,可能会伴随着热能变化 |
3.下列说法正确的是( )
| A. | 常温下,苯酚易溶于水 | |
| B. | 苯酚俗称石炭酸,具有微弱的酸性,能与碳酸钠溶液反应 | |
| C. | 能与FeCl3溶液作用显紫色的有机物一般含有酚羟基 | |
| D. | 洒落皮肤上的苯酚可以用氢氧化钠稀溶液洗涤 |
10.某同学按下列步骤配制500mL 0.200mol•L-1 Na2CO3溶液,请回答有关问题.
你认为按上述步骤配制的Na2CO3溶液的浓度是否为0.200mol•L-1,请说明理由.
| 实验步骤 | 有关问题 |
| (1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为10.6g. |
| (2)称量Na2CO3固体 | 称量过程中主要用到的仪器是托盘天平、砝码、药匙. |
| (3)将Na2CO3加入100mL烧杯中 | 为加快溶解速率,可采取的措施是用玻棒搅拌或加热 |
| (4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应采取的措施是用玻璃棒引流 |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是当加水璃刻度线1-2cm时改用胶头璃管加水至凹液面与刻度线相切 |
8.下列关于离子键、共价键的叙述中正确的是( )
| A. | 非极性键只存在于双原子的单质分子(如Cl2)中 | |
| B. | 在共价化合物里,可能存在离子键 | |
| C. | 在离子化合物里,只存在离子键,没有共价键 | |
| D. | 化学反应的实质是旧键的断裂,新键的形成 |
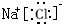 ;
;