题目内容
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O═2NO+HNO3+9HF.下列有关该反应的说法正确的是( )
| A、NO是氧化产物 |
| B、NF3是氧化剂,H2O是还原剂 |
| C、氧化剂与还原剂的物质的量之比为2:1 |
| D、若生成0.2 mol HNO3,则转移0.2 mol电子 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:3NF3+5H2O=2NO+HNO3+9HF反应中,只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,从化合价的变化的角度分析氧化还原反应.
解答:
解:A.生成的NO时,N元素的化合价降低,得到电子被还原,则NO为还原产物,故A错误;
B.只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,故B错误;
C.NF3生成NO,被还原,NF3生成HNO3,被氧化,氧化剂与还原剂的物质的量之比为2:1,故C正确;
D.生成0.2molHNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,故D错误;
故选C.
B.只有N元素的化合价发生变化,NF3既是氧化剂又是还原剂,故B错误;
C.NF3生成NO,被还原,NF3生成HNO3,被氧化,氧化剂与还原剂的物质的量之比为2:1,故C正确;
D.生成0.2molHNO3,转移的电子的物质的量为0.2mol×(5-3)=0.4mol,故D错误;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素化合价的升降为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意从化合价的角度分析,题目难度不大.

练习册系列答案
相关题目
下列各组溶液,不用试剂无法鉴别的是( )
| A、NaOH和明矾 |
| B、氨水和AgNO3 |
| C、NaAlO2和HCl |
| D、Na2SO4和BaCl2 |
(CH3CH2)2CHCH3的正确命名是( )
| A、2-乙基丁烷 |
| B、3-乙基丁烷 |
| C、2-甲基戊烷 |
| D、3-甲基戊烷 |
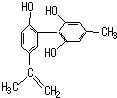 坚决反对运动员服用兴奋剂,是我国支持“人文奥运”的重要体现.某种兴奋剂的结构简式如图所示,有关该物质及其溶液的说法不正确的是( )
坚决反对运动员服用兴奋剂,是我国支持“人文奥运”的重要体现.某种兴奋剂的结构简式如图所示,有关该物质及其溶液的说法不正确的是( )| A、该分子中所有氢原子不可能在同一个平面上 |
| B、1 mol该物质与H2反应时,最多消耗7 molH2 |
| C、加入FeCl3溶液呈紫色,因为该物质属于酚类物质 |
| D、滴入酸性高锰酸钾溶液,紫色褪去,可证明结构中存在碳碳双键 |
下列反应中,可能高温正向自发,低温逆向自发的是( )
| A、NH3(g)+HCI(g)=NH4Cl(s) |
| B、CaCO3(s)=CaO(s)+CO2(g) |
| C、4Al(s)+3O2(g)=2Al2O3(s) |
| D、HCI(aq)+NaOH(aq)=NaCl(aq)+H2O(I) |
以下化学用语正确的是( )
| A、乙炔的最简式:CH≡CH |
| B、乙酸的结构简式:CH3CH2COOH |
C、CO2的电子式: |
| D、乙酸乙酯的分子式:C4H8O2 |
下列事实与结论相符且正确的是( )
| A、100 mL 0.1 mol?L-1AlCl3溶液中含有Al3+数目为0.01NA(NA代表阿伏加德罗常数) |
| B、Ksp(BaSO4)=1.07×10-10,Ksp(BaCO3)=2.58×10-9,所以不能将BaSO4转化为BaCO3 |
| C、常温下,pH=11的NaOH溶液和pH=3的CH3COOH溶液等体积混合,溶液pH<7 |
| D、0.1 mol?L-1 Na2CO3溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |