题目内容
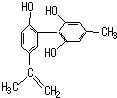 坚决反对运动员服用兴奋剂,是我国支持“人文奥运”的重要体现.某种兴奋剂的结构简式如图所示,有关该物质及其溶液的说法不正确的是( )
坚决反对运动员服用兴奋剂,是我国支持“人文奥运”的重要体现.某种兴奋剂的结构简式如图所示,有关该物质及其溶液的说法不正确的是( )| A、该分子中所有氢原子不可能在同一个平面上 |
| B、1 mol该物质与H2反应时,最多消耗7 molH2 |
| C、加入FeCl3溶液呈紫色,因为该物质属于酚类物质 |
| D、滴入酸性高锰酸钾溶液,紫色褪去,可证明结构中存在碳碳双键 |
考点:有机物的结构和性质
专题:
分析:该有机物含有酚羟基、双键等,可与高锰酸钾发生氧化反应,含有C=C官能团,可发生加成、氧化反应,结合甲基的结构特征判断有机物的空间结构特点.
解答:
解:A.结构中含2个甲基,为四面体结构,则该分子中所有氢原子不可能在同一个平面上,故A正确;
B.两个苯环、一个C=C可发生加成反应,则1 mol该物质与H2反应时,最多消耗7 molH2,故B正确;
C.含酚-OH,加入FeCl3溶液呈紫色,因为该物质属于酚类物质,故C正确;
D.能使酸性KMnO4褪色的官能团有酚羟基、C=C、苯环上的甲基,则滴入酸性高锰酸钾溶液,紫色褪去,不能证明结构中存在碳碳双键,故D错误;
故选D.
B.两个苯环、一个C=C可发生加成反应,则1 mol该物质与H2反应时,最多消耗7 molH2,故B正确;
C.含酚-OH,加入FeCl3溶液呈紫色,因为该物质属于酚类物质,故C正确;
D.能使酸性KMnO4褪色的官能团有酚羟基、C=C、苯环上的甲基,则滴入酸性高锰酸钾溶液,紫色褪去,不能证明结构中存在碳碳双键,故D错误;
故选D.
点评:本题考查有机物结构与性质,为高频考点,把握有机物官能团的性质进行判断,易错点为D,注意有机物空间结构的分析,题目难度中等.

练习册系列答案
相关题目
铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):下列计算结果正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属/g | 18.0 | 9.6 | 0 | 0 |
| NO体积/mL | 2240 | 4480 | 6720 | v |
| A、硝酸的浓度为6mol/L |
| B、①中溶解了5.6gFe |
| C、②中溶解了9.6gCu |
| D、④中v=8960 |
下列说法正确的是( )
| A、通常情况下,植物油的熔点比动物油的熔点高 |
| B、人体中,油脂主要在胃中被消化吸收 |
| C、质量相同的油脂和葡萄糖完全氧化时,油脂产生的能量比葡萄糖的高 |
| D、油脂在人体中,能够被氧化放出能量的主要是油脂水解生成的甘油 |
实验室保存下列试剂的试剂瓶可以用橡胶塞的是( )
| A、溴水 | B、酸性高锰酸钾溶液 |
| C、纯碱溶液 | D、四氯化碳 |
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O═2NO+HNO3+9HF.下列有关该反应的说法正确的是( )
| A、NO是氧化产物 |
| B、NF3是氧化剂,H2O是还原剂 |
| C、氧化剂与还原剂的物质的量之比为2:1 |
| D、若生成0.2 mol HNO3,则转移0.2 mol电子 |
已知:金属铁(含杂质碳)在酸性溶液中发生析氢腐蚀,总反应方程式为:Fe+2H+═Fe2++H2↑;铁在中性或碱性溶液中发生吸氧腐蚀,总反应式为:4Fe+3O2+6H2O═4Fe(OH)3↓.某课外活动小组,将剪下的一块铁片放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按图装置进行实验,数分钟后观察,下列现象不可能出现的是( )
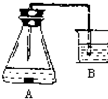

| A、铁被腐蚀 |
| B、B中导气管里形成一段水柱 |
| C、金属片剪口处变红 |
| D、B中导气管中产生气泡 |
下列方程式属于水解反应的是( )
| A、HCO3-+H2O?H3O++CO32- |
| B、H2O+H2O?H3O++H+ |
| C、HCO3-+OH-=H2O+CO32- |
| D、CO32-+H2O?HCO3-+OH- |