题目内容
15.下列方程式正确的是( )| A. | 用氯胺处理自来水:NH2Cl+H2O?NH2OH+HCl | |
| B. | 在含有Mg2+、HCO3-的自来水中加入过量的澄清石灰水:Ca2++Mg2++2OH-+2HCO3-═CaCO3↓+MgCO3↓+2H2O | |
| C. | 长时间煮沸含Mg2+、HCO3-的自来水:Mg2++2HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2CO2↑ | |
| D. | Na2FeO4既是混凝剂、又可作消毒剂,作混凝剂的作用原理为:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
分析 A.氯胺处理自来水应生成NH3和HClO;
B.Mg2+与过量的澄清石灰水反应,生成Mg(OH)2;
C.加热碳酸氢镁溶液生成二氧化碳和氢氧化镁;
D.三价铁离子水解为可逆反应.
解答 解:A.氯胺处理自来水应生成NH3和HClO,离子方程式:NH2Cl+H2O?NH3+HClO,故A错误;
B.Mg2+与过量的澄清石灰水反应,生成Mg(OH)2,故B错误;
C.加热碳酸氢镁溶液生成二氧化碳和氢氧化镁,化学方程式:Mg2++2HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2CO2↑,故C正确;
D.Na2FeO4既是混凝剂、又可作消毒剂,作混凝剂的作用原理为:Fe3++3H2O?Fe(OH)3(胶体)+3H+,故D错误;
故选:C.
点评 本题考查了化学方程式、离子方程式的书写,明确物质的性质及发生的反应是解题关键,注意盐类水解反应规律,题目难度中等.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
5.不能使热的CuO表面变红的是( )
| A. | CH3CH(OH)CH3 | B. | (CH3)3COH | C. | CH3CH(OH)CH2CH3 | D. | (CH3)3CCH2OH |
6.向amol/L的氨水中加入等体积b mol•L-1的盐酸,下列关系错误的是( )
| A. | 当a=b时,c(H+)=c(OH-)+c(NH3•H2O) | |
| B. | 当a>b时,c(NH4+)+c(NH3•H2O)>c(Cl-) | |
| C. | 当a<b时,c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | 当a与b为任意比时,c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
3.常温下向25mL 0.1mol.L-1NaOH溶液中逐滴滴加0.2mol•L-1的HN3(叠氮酸)溶液,pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的Ka=10-4.7).下列说法正确的是( )


| A. | 水电离出的c(H+):A点小于B点 | |
| B. | 在B点,离子浓度大小为c(OH-)>c(H+)>c(Na+)>c(N3-) | |
| C. | 在C点,滴加的V(HN3)=12.5 mL | |
| D. | 在D点,c(Na+)=2c(HN3)+2 c(N3-) |
10.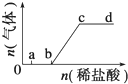 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )| A. | a点对应的溶液中:Na+、OH-、SO42-、NO3- | |
| B. | b点对应的溶液中:Al3+、Fe3+、SCN-、Cl- | |
| C. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应的溶液中:SO32-、Na+、Cl-、NO3- |
7.下列说法不正确的( )
| A. | 生铁和钢都属于合金 | |
| B. | 明矾可用作混凝剂去除水中的悬浮物 | |
| C. | 食盐水、稀豆浆、糖水都能产生丁达尔效应 | |
| D. | 以次氯酸钠为有效成分的漂白液可为泳池消毒 |
4.下列说法正确的是( )
| A. | c(H+)<c(OH-)的溶液一定显碱性 | B. | pH=6的溶液一定显酸性 | ||
| C. | pH=7的溶液一定显中性 | D. | Kw只适用于纯水 |

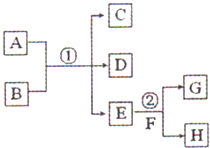 在如图各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).回答下列问题:
在如图各变化中,E为无色无味的液体(常温下),F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).回答下列问题: