题目内容
7.下列说法不正确的( )| A. | 生铁和钢都属于合金 | |
| B. | 明矾可用作混凝剂去除水中的悬浮物 | |
| C. | 食盐水、稀豆浆、糖水都能产生丁达尔效应 | |
| D. | 以次氯酸钠为有效成分的漂白液可为泳池消毒 |
分析 A.生铁和钢均为Fe的合金;
B.明矾中铝离子水解生成胶体,具有吸附性;
C.丁达尔效应为胶体的性质,而食盐水和糖水为溶液;
D.次氯酸钠具有强氧化性.
解答 解:A.生铁和钢均为Fe的合金,还含碳等,故A正确;
B.明矾中铝离子水解生成胶体,具有吸附性,则明矾可用作混凝剂去除水中的悬浮物,故B正确;
C.丁达尔效应为胶体的性质,而食盐水和糖水为溶液,只有稀豆浆能产生丁达尔效应,故C错误;
D.次氯酸钠具有强氧化性,则以次氯酸钠为有效成分的漂白液可为泳池消毒,故D正确;
故选C.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应及性质与用途的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18. 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
)为原料制备2-氯丁烷
( ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
以下是实验步骤:
步骤1:在圆底烧瓶内放入无水ZnC12和12mol.L一1浓盐酸,充分溶解、冷却,再加入2一丁
醇,加热一段时间.
步骤2:将反应混合物移至蒸馏装置内,蒸馏并收集115℃以下馏分.
步骤3:从馏分中分离出有机相,依次用蒸馏水、5%NaoH溶液、蒸馏水
洗涤,再加入CaCl2固体,放置一段时间后过滤.
步骤4:滤液经进一步精制得产品
(1)加入烧瓶的物质中,有一种是催化剂,该物质是无水ZnCl2.
(2)反应装置中冷凝管的作用是冷凝回流提高原料利用率,烧杯内所盛液体可以是水或碱液.
(3)用NaoH溶液洗涤时操作要迅速,其原因是防止2-氯丁烷水解减少2-氯丁烷挥发,第二次用蒸馏水
洗涤的目的是除去残留的氢氧化钠.
(4)步骤4精制过程中不需使用的仪器是ad.
a.布氏漏斗b.抽滤瓶c.蒸馏烧瓶d.冷凝管.
 实验室以2一丁醇(
实验室以2一丁醇( )为原料制备2-氯丁烷
)为原料制备2-氯丁烷(
 ),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:
),实验装置如图所示(夹持、加热装置省去未画)相关数据见下表:| 物质 | 熔点 (℃) | 沸点(℃) |
| 2-丁醇 | -114.7 | 99.5 |
| 2-氯乙烷 | -131.3 | 68.2 |
步骤1:在圆底烧瓶内放入无水ZnC12和12mol.L一1浓盐酸,充分溶解、冷却,再加入2一丁
醇,加热一段时间.
步骤2:将反应混合物移至蒸馏装置内,蒸馏并收集115℃以下馏分.
步骤3:从馏分中分离出有机相,依次用蒸馏水、5%NaoH溶液、蒸馏水
洗涤,再加入CaCl2固体,放置一段时间后过滤.
步骤4:滤液经进一步精制得产品
(1)加入烧瓶的物质中,有一种是催化剂,该物质是无水ZnCl2.
(2)反应装置中冷凝管的作用是冷凝回流提高原料利用率,烧杯内所盛液体可以是水或碱液.
(3)用NaoH溶液洗涤时操作要迅速,其原因是防止2-氯丁烷水解减少2-氯丁烷挥发,第二次用蒸馏水
洗涤的目的是除去残留的氢氧化钠.
(4)步骤4精制过程中不需使用的仪器是ad.
a.布氏漏斗b.抽滤瓶c.蒸馏烧瓶d.冷凝管.
15.下列方程式正确的是( )
| A. | 用氯胺处理自来水:NH2Cl+H2O?NH2OH+HCl | |
| B. | 在含有Mg2+、HCO3-的自来水中加入过量的澄清石灰水:Ca2++Mg2++2OH-+2HCO3-═CaCO3↓+MgCO3↓+2H2O | |
| C. | 长时间煮沸含Mg2+、HCO3-的自来水:Mg2++2HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2CO2↑ | |
| D. | Na2FeO4既是混凝剂、又可作消毒剂,作混凝剂的作用原理为:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
12.已知16S和30Se位于同一主族,下列关系正确的是( )
| A. | 热稳定性:HF>HCl>H2S | B. | 原子半径:Br>Se>Cl | ||
| C. | 还原性:S2->Se2->Cl- | D. | 酸性:HBrO4>HClO4>H2SO4 |
17.向某晶体的溶液中加入Fe2+后溶液无明显变化,再滴加几滴氯水后,混合液出现血红色,由此得出的下列结论错误的是( )
| A. | Fe2+不能与SCN-形成血红色化合物 | B. | 该晶体中一定含有SCN- | ||
| C. | Fe3+的氧化性比氯气的氧化性强 | D. | Fe2+被氯气氧化成Fe3+ |
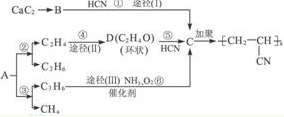 人造羊毛的主要成分为聚丙烯腈
人造羊毛的主要成分为聚丙烯腈 ,此物质可由以下三种途径合成,已知A是石油分馏的一种产品.
,此物质可由以下三种途径合成,已知A是石油分馏的一种产品.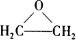 .
. 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应: