题目内容
在如图分子中,处于同一平面上的原子数最多可能有( )


| A、12个 | B、14个 |
| C、18个 | D、20个 |
考点:常见有机化合物的结构
专题:有机化学基础
分析:在常见的有机化合物中,甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行共线、共面分析判断,注意单键可以旋转.
解答:
解:在 分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,
分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,
故选D.
 分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,
分子中,甲基中C原子处于苯中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在苯环平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故选D.
点评:本题考查有机物结构中共面、共线问题,关键是空间想象,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,单键可以旋转.

练习册系列答案
相关题目
足量的两份铝粉分别与等体积的盐酸和NaOH溶液反应,同温同压下产生的气体体积比为1:1,则盐酸和NaOH溶液的物质的量浓度之比为( )
| A、2:3 | B、3:1 |
| C、1:2 | D、1:1 |
甲醇燃料电池(DMFC)可用于笔记本电脑、汽车、遥感通讯设备等,它的一极通入甲醇,一极通入氧气;电解质是质子交换膜,它能传导氢离子(H+).电池工作时,甲醇被氧化为二氧化碳和水,氧气在电极上的反应是O2+4H++4e-═2H2O.下列叙述中不正确的是( )
| A、负极的反应式为CH3OH+H2O-6e-═CO2↑+6H+ |
| B、电池的反应方程式是2CH3OH+3O2═2CO2+4H2O |
| C、电池工作时,H+由正极移向负极 |
| D、电池工作时,电子从通入甲醇的一极流出,经外电路再从通入氧气的一极流入 |
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示.下列说法中正确的是( )
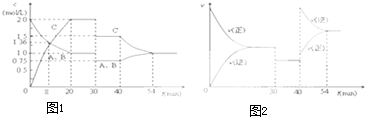

| A、第8min时 A的反应速率为0.08mol?L-1?min-1 |
| B、在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 |
| C、30min时改变的条件是降低温度,40min时改变的条件是升高温度 |
| D、反应方程式中的x=1,且正反应为放热反应 |
少量钠着火时,可用来灭火的物质或器材是( )
| A、煤油 | B、CO2 |
| C、砂土 | D、水 |
已知反应:①101kPa时,C(s)+
O2(g)=CO(g)△H1=-110.5kJ?mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H2=-57.3kJ?mol-1下列结论正确的是( )
| 1 |
| 2 |
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H2=-57.3kJ?mol-1下列结论正确的是( )
| A、若碳的燃烧热用△H3来表示,则△H3<△H1 |
| B、若碳的燃烧热用△H3来表示,则△H3>△H1 |
| C、浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ?mol-1 |
| D、稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
相同状况下,20mL气体A2和10mL气体B2恰好化合生成20mL气体C,则C的化学式为( )
| A、AB |
| B、AB2 |
| C、A2B |
| D、A2B3 |
A、B、C都是有机化合物,有如下转化关系:A
B
C,A的相对分子质量比B小18,B的相对分子质量比C大2,A是衡量一个国家石油化工业水平的重要标志之一的一种常见气体.以下说法正确的是( )
| +水 |
| 消去 |
| 催化氧化 |
| A、A是乙炔,B是乙醇 |
| B、A是乙烯,C是乙醛 |
| C、A是乙烯,C是乙醇 |
| D、A是环己烷,C是苯 |