题目内容
现有钠、镁、铝各1mol,分别与100mL 5.0mol/L盐酸充分反应后,所得同温、同压下的H2体积关系正确的是( )
| A、产生H2体积相等 |
| B、铝产生H2最多,钠产生H2最少 |
| C、钠产生H2最多,铝产生H2最少 |
| D、钠产生H2最多,镁、铝产生H2相等 |
考点:化学方程式的有关计算
专题:计算题
分析:Na与盐酸反应,2Na+2HCl=2NaCl+H2↑,盐酸不足,发生反应2Na+2H2O=2NaOH+H2↑,根据关系式2Na~H2↑计算生成氢气的物质的量;
Mg、Al与盐酸发生反应:Mg+2HCl=MgCl2+H2↑,2Al+6HCl=2AlCl3+3H2↑,计算HCl的物质的量,进行过量计算,根据不足量的物质计算生成氢气的物质的量;
相同条件下,体积之比等于物质的量之比,据此判断.
Mg、Al与盐酸发生反应:Mg+2HCl=MgCl2+H2↑,2Al+6HCl=2AlCl3+3H2↑,计算HCl的物质的量,进行过量计算,根据不足量的物质计算生成氢气的物质的量;
相同条件下,体积之比等于物质的量之比,据此判断.
解答:
解:100ml 5.0mol/L的盐酸中n(HCl)=0.1L×5.0mol/L=0.5mol,
Na与盐酸反应,2Na+2HCl=2NaCl+H2↑,盐酸不足,发生反应2Na+2H2O=2NaOH+H2↑,
由关系式2Na~H2↑,可知1molNa反应生成氢气的物质的量为1mol×
=0.5mol,
Mg+2HCl=MgCl2+H2↑
1mol 2mol
故Mg剩余,盐酸不足,故生成氢气为0.5mol×
=0.25mol,
2Al+6HCl=2AlCl3+3H2↑
1mol 3mol
故Al剩余,盐酸不足,故生成氢气为0.5mol×
=0.25mol,
由上述分析,相同条件下,钠产生H2最多,镁、铝产生H2相等,
故选D.
Na与盐酸反应,2Na+2HCl=2NaCl+H2↑,盐酸不足,发生反应2Na+2H2O=2NaOH+H2↑,
由关系式2Na~H2↑,可知1molNa反应生成氢气的物质的量为1mol×
| 1 |
| 2 |
Mg+2HCl=MgCl2+H2↑
1mol 2mol
故Mg剩余,盐酸不足,故生成氢气为0.5mol×
| 1 |
| 2 |
2Al+6HCl=2AlCl3+3H2↑
1mol 3mol
故Al剩余,盐酸不足,故生成氢气为0.5mol×
| 1 |
| 2 |
由上述分析,相同条件下,钠产生H2最多,镁、铝产生H2相等,
故选D.
点评:本题考查根据方程式的计算,涉及过量计算,难度不大,注意Na与酸的反应,盐酸不足时Na与水反应.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
在25℃下,将m mol?L-1的醋酸溶液与n mol?L-1的氢氧化钠溶液等体积混合,恰好使反应后的溶液呈中性,则下列观点正确的是( )
| A、反应后的溶液中:c(Na+)>c(CH3COO-) | ||
| B、反应前溶液的物质的量浓度:m=n | ||
| C、反应后的溶液中:c(CH3COO-)+c(CH3COOH)=m mol?L-1 | ||
D、该温度下,醋酸的电离平衡常数的表达式为:Ka=
|
a克铁粉与含有硫酸的硫酸铜溶液完全反应后,得到a克铜,则参加反应的硫酸铜与硫酸的物质的量之比是( )
| A、1:7 | B、7:1 |
| C、7:8 | D、8:7 |
下列实验操作中错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时不应将溶液直接蒸干 |
| D、食盐应放在滤纸上称量 |
下列各组有机物,一定属于同系物的是( )
A、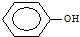 和 和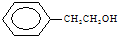 |
| B、最简式相同的有机物 |
| C、丙酸丙酯和高级脂肪甘油脂 |
| D、分子组成为CnH2n+2和CmH2m+2(m≠n)的两种烃 |
电解质是( )
| A、导电性很强的物质,在任何情况下均能导电 |
| B、在溶于水或熔融状态下能导电的化合物 |
| C、在溶于水或熔融状态下全部电离的化合物 |
| D、可溶性盐类、酸类和碱类等化合物 |
下列电离方程式错误的是( )
| A、CaCl2=Ca2++2Cl- |
| B、NaHSO4=Na++H++SO42- |
| C、H2CO3=2H++CO32- |
| D、HNO3=H++NO3- |
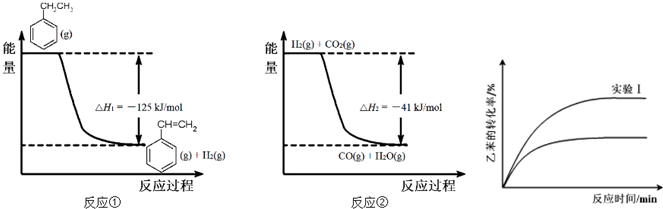
 (g)+CO2(g)?
(g)+CO2(g)? (g)+CO(g)+H2O(g)的△H=
(g)+CO(g)+H2O(g)的△H= )的影响,并设计了如下实验:
)的影响,并设计了如下实验: