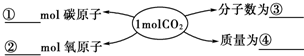
题目内容
Mg-AgCl电池是一种用海水激活的一次电池,在军事上用作电动鱼雷的电源.电池的总反应可表示为:Mg+2AgCl═MgCl2+2Ag.下列关于该电池的说法错误的是( )
| A、该电池工作时,正极反应为:2AgCl+2e一═2C1一+2Ag |
| B、镁电极做该电池负极,负极反应为:Mg-2e一═Mg2+ |
| C、有24g Mg被氧化时,可还原得到108gAg |
| D、装备该电池的鱼雷在水中行进时,海水作为电解质溶液 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、原电池中,发生得电子的还原反应的极是正极;
B、在原电池的负极上发生失电子的氧化反应;
C、根据电极反应式结合电子守恒来回答判断;
D、根据信息:电池是一种能被海水激活的一次性贮备电池来回答判断.
B、在原电池的负极上发生失电子的氧化反应;
C、根据电极反应式结合电子守恒来回答判断;
D、根据信息:电池是一种能被海水激活的一次性贮备电池来回答判断.
解答:
解:A、由电池反应方程式看出,Mg是还原剂、AgCl是氧化剂,故金属Mg作负极,正极反应为:2AgCl+2e-═2C1-+2Ag,故A正确;
B、金属Mg作负极,其电极反应式为:Mg-2e-=Mg2+,故B正确;
C、电极反应式:Mg-2e-=Mg2+,24g Mg即1mol被氧化时,转移电子是2mol,正极反应为:2AgCl+2e-═2C1-+2Ag,可还原得到216gAg,故C错误;
D、因为该电池能被海水激活,海水可以作为电解质溶液,故D正确.
故选C.
B、金属Mg作负极,其电极反应式为:Mg-2e-=Mg2+,故B正确;
C、电极反应式:Mg-2e-=Mg2+,24g Mg即1mol被氧化时,转移电子是2mol,正极反应为:2AgCl+2e-═2C1-+2Ag,可还原得到216gAg,故C错误;
D、因为该电池能被海水激活,海水可以作为电解质溶液,故D正确.
故选C.
点评:总结题技巧总结:电极类型的判断首先在明确属于电解池还是原电池基础上来分析的,原电池对应的是正、负两极,电解池对应的阴、阳两极,根据元素价态变化找出氧化剂与还原产物.

练习册系列答案
 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图:
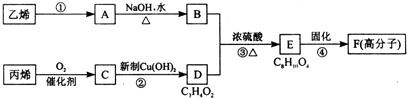
关于该过程的相关叙述正确的是( )

关于该过程的相关叙述正确的是( )
| A、反应④的反应类型是缩聚反应 |
| B、物质A是卤代烃 |
| C、物质B催化氧化后可以得到乙醛 |
| D、1 mol物质D最多可以消耗2 mol NaOH |
下列物质既能跟硫酸反应,又能跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al.
| A、①②③④ | B、①和③ |
| C、③和④ | D、①和④ |
超临界流体(Supercritical Fluid)是温度和压力同时高于临界值的流体,也即压缩到具有接近液体密度的气体,是物质介于气态和液态之间的一种新的状态.目前应用最广的是超临界二氧化碳,在中药、香料的萃取分离以及作为溶剂、发泡剂取代氟利昂等具有重要价值.下列有关说法中错误的是( )
| A、超临界二氧化碳与CO2的物理性质不同,化学性质相同 |
| B、超临界二氧化碳可能是一种原子晶体 |
| C、用超临界二氧化碳溶解萃取物质,符合绿色化学的思想 |
| D、用超临界二氧化碳代替氟利昂可减轻对臭氧层的破坏 |
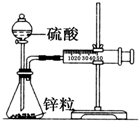 按如图安装好实验装置(装置气密性良好),在锥形瓶内盛6.5g锌粒(相对原子质量Zn-65),通过分液漏斗加入40mL2.5mol/L的硫酸溶液,将产生的H2收集在一个注射器中,用时10s时恰好收集到标准状况下的H244.8mL.下列说法不正确的是( )
按如图安装好实验装置(装置气密性良好),在锥形瓶内盛6.5g锌粒(相对原子质量Zn-65),通过分液漏斗加入40mL2.5mol/L的硫酸溶液,将产生的H2收集在一个注射器中,用时10s时恰好收集到标准状况下的H244.8mL.下列说法不正确的是( )| A、忽略锥形瓶内溶液体积的变化,用H+来表示10s内该反应的速率0.01mol/(L?s) |
| B、忽略锥形瓶内溶液体积的变化,用Zn2+来表示10s内该反应的速率0.01mol/(L?s) |
| C、用锌粒来表示10s内该反应的速率为0.013g/s |
| D、用H2来表示10s内该反应的速率为0.0002mol/s |
设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A、1mol?L -1的NaClO溶液中含有ClO-的数目为NA |
| B、常温常压下,分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| C、标准状况下,11.2 L CH3CH2OH 中含有的氢原子数目为3NA |
| D、室温下,1L pH=13的Ba(OH)2溶液中,OH-离子数目为0.2NA |