题目内容
化学与能源开发、环境保护、资源利用等密切相关.下列有关说法不正确的是( )
| A、将开采出的煤通过干馏、气化、液化等多种途径实现其综合利用 |
| B、氢气是清洁能源,工业上可用电解水法来开发氢能源 |
| C、向污水中投放明矾,利用生成的胶体净水:Al3++3H2O?Al(OH3)(胶体)+3H+ |
| D、“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 |
考点:常见的生活环境的污染及治理,清洁能源,盐类水解的应用
专题:化学应用
分析:A.煤综合利用,可以减少污染物的排放;
B.电解水法来开发氢能源,成本太高;
C.明矾净水是因为水解生成了氢氧化铝胶体具有吸附性;
D.氮氧化合物与“光化学烟雾”、“硝酸型酸雨”的形成都有关.
B.电解水法来开发氢能源,成本太高;
C.明矾净水是因为水解生成了氢氧化铝胶体具有吸附性;
D.氮氧化合物与“光化学烟雾”、“硝酸型酸雨”的形成都有关.
解答:
解:A.煤通过干馏、气化、液化等多种途径实现其综合利用,可以减少污染物的排放,故A正确;
B.工业上不用电解水法来开发氢能源,因为成本太高,故B错误;
C.明矾净水是因为水解生成了氢氧化铝胶体具有吸附性,故C正确;
D.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关,故D正确;
故选B.
B.工业上不用电解水法来开发氢能源,因为成本太高,故B错误;
C.明矾净水是因为水解生成了氢氧化铝胶体具有吸附性,故C正确;
D.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关,故D正确;
故选B.
点评:本题考查化学与环境、资源等知识,侧重于基础知识的考查,有利于培养学生的良好的学科素养和提高学习的积极性,难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
中药狼把草的成分之一M具有清炎杀菌作用,M的结构如图所示: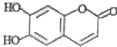 ,下列叙述不正确的是( )
,下列叙述不正确的是( )
 ,下列叙述不正确的是( )
,下列叙述不正确的是( )| A、该物质在酸性条件下加热可以水解 |
| B、1mol M最多能与3mol Br2发生反应 |
| C、M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 |
| D、1mol M与足量NaHCO3反应能生成2mol CO2 |
下列化学用语正确的是( )
A、中子数为8的碳原子:
| ||
B、氟离子的结构示意图: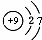 | ||
C、甲烷分子的结构式: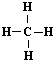 | ||
D、N2的电子式: |
有a、b、c、d 4种金属,将a与b用导线连接起来,浸入NaCl溶液中,b不易腐蚀;将a、d分别投入等浓度的盐酸中,d比a反应剧烈;将铜浸在b盐溶液中,无明显变化;如果把铜浸入c的盐溶液中,有金属c析出.据此判断它们的活动性由强到弱的顺序是( )
| A、d>c>a>b |
| B、b>a>d>c |
| C、d>b>a>c |
| D、d>a>b>c |
下列有关物质性质的说法错误的是( )
| A、热稳定性:HCl>HI |
| B、原子半径:Na>Mg |
| C、酸性:H2SO3>H2SO4 |
| D、结合质子能力:S2->Cl- |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA |
| B、将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积约为22.4L |
| C、在反应KClO4+8HCl═KCl+4Cl2↑+4H2O中,每生成4mol Cl2转移的电子数为8NA |
| D、25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA |
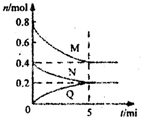 在容积为2L的恒容的密闭容器中,一定温度下,发生反应:aM(g)+bN(g)?cQ(g).气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )
在容积为2L的恒容的密闭容器中,一定温度下,发生反应:aM(g)+bN(g)?cQ(g).气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )A、该温度下此反应的平衡常数的值K=
| ||
| B、该反应前5min的平均速率:v(N)=0.002mol?L-1?min-1 | ||
| C、在5min时,再向体系中充入少量He,重新达到平衡前v(正)>v(逆) | ||
| D、若开始时向容器中充入2mol M和1mol N,达到平衡时,M的体积分数小于50% |