题目内容
利用碱性氧化性溶液的氧化作用,在钢铁表面形成一层Fe3O4(也可表示为FeFe2O4)薄膜,保护内部金属免受腐蚀,这种方法叫做烤蓝.烤蓝时发生如下反应:下列说法中正确的是( )
①3Fe+NaNO2+5NaOH═3Na2FeO2+H2O+NH3↑
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH(未配平)
③Na2FeO2+Na2Fe2O4+2H2O═Fe3O4+4NaOH.
①3Fe+NaNO2+5NaOH═3Na2FeO2+H2O+NH3↑
②Na2FeO2+NaNO2+H2O═Na2Fe2O4+NH3↑+NaOH(未配平)
③Na2FeO2+Na2Fe2O4+2H2O═Fe3O4+4NaOH.
| A、Fe3O4既可看做是氧化物,又可看做是铁盐 |
| B、反应②配平后,H2O的化学计量数为3 |
| C、反应③中,Na2Fe2O4是氧化剂,Na2FeO2是还原剂 |
| D、碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强 |
考点:氧化还原反应
专题:
分析:A.根据氧化物及盐的概念,结合其可表示为FeFe2O4来分析;
B.根据电子守恒来分析;
C.反应③中各元素的化合价不变;
D.根据氧化剂氧化性大于氧化产物的氧化性判断.
B.根据电子守恒来分析;
C.反应③中各元素的化合价不变;
D.根据氧化剂氧化性大于氧化产物的氧化性判断.
解答:
解:A.氧化物中只有两种元素,其一为氧元素,则属于氧化物,可表示为FeFe2O4,由金属阳离子与酸根离子构成,则属于盐,故A正确;
B.Fe元素由+2升高为+3,N元素由+3降低为-3,由电子守恒及质量守恒定律可知反应为6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3↑+7NaOH,H2O的化学计量数为5,故B错误;
C.反应③中各元素的化合价不变,不属于氧化还原反应,故C错误;
D.氧化还原反应中,氧化剂氧化性大于氧化产物的氧化性,由此可判断碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强,故D正确;
故选AD.
B.Fe元素由+2升高为+3,N元素由+3降低为-3,由电子守恒及质量守恒定律可知反应为6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3↑+7NaOH,H2O的化学计量数为5,故B错误;
C.反应③中各元素的化合价不变,不属于氧化还原反应,故C错误;
D.氧化还原反应中,氧化剂氧化性大于氧化产物的氧化性,由此可判断碱性条件下,NaNO2的氧化性比Na2FeO2、Na2Fe2O4都强,故D正确;
故选AD.
点评:本题考查氧化还原反应,注意利用元素的化合价及相关信息来解答,明确元素的化合价变化是解答的关键,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
化学式为C5H12O的有机物,经测定知其分子中含有两个-CH3,两个-CH2-,一个 和一个-OH,则它们的可能结构有( )
和一个-OH,则它们的可能结构有( )
 和一个-OH,则它们的可能结构有( )
和一个-OH,则它们的可能结构有( )| A、5种 | B、3种 | C、2种 | D、4种 |
下列装置图或曲线图与对应的叙述相符的是( )
A、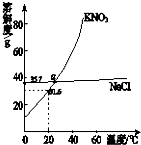 固体KNO3中混有NaCl,可用重结晶进行提纯 |
B、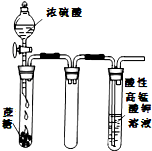 酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
C、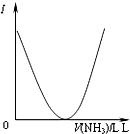 可表示乙酸溶液中通入氨气至过量过程中溶液导电性(I )的变化 |
D、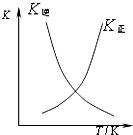 可表示在恒容密闭容器中反应“2SO2(g)+O2(g)═2SO3(g)△H<0”的平衡常数K正、K逆随温度 |
据报道,锌-空气电池将会成为21世纪理想动力源.在碱性溶液中该电池总反应可表示为:2Zn+4NaOH+O2=2Na2ZnO2+2H2O,下列有关锌-空气电池说法正确的是( )
| A、每生成1mol Na2ZnO2转移4mol电子 |
| B、负极反应式为:Zn+4OH--2e-=ZnO22-+2 H2O |
| C、电池工作时,溶液中的Na+向负级移动 |
| D、碱性或酸性电解液中,该电池正极反应式相同 |
如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )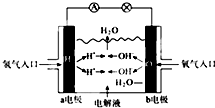

| A、a电极是负极 |
| B、b电极的电极反应为O2+4e-+2H2O=4OH- |
| C、工作时,溶液中阴离子向正极移动,阳离子向负极移动 |
| D、此电池能将化学能转化为电能 |
两种元素X、Y,其原子核外电子层数分别为a、b,最外层电子数分别为m、n.下列说法错误的是( )
| A、若8>m>3,则X必定为主族元素 |
| B、若Y的气态氢化物化学式为YHn,且b=4,则该氢化物为非极性分子 |
| C、若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y>X |
| D、若a=b=3,8>m>n>b,则元素非金属性:X>Y |
下列说法正确的是( )
| A、蒸馏时,通入冷凝管的水从其上口流进,下口流出 |
| B、一束平行光照射CuSO4溶液时,从侧面可看到光亮的通路 |
| C、电解质溶液导电的原因是因为有自由移动的离子 |
| D、将饱和的FeCl3溶液滴入沸腾的NaOH溶液中可制得氢氧化铁胶体 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,11.2L氯仿中含有的C-Cl键的数目为1.5NA |
| B、标准状况下,30g NO和16g O2混合所生成的气体分子数为NA |
| C、某温度时,1L pH=6的纯水中含有1.0×10-6NA个H+ |
| D、28g铁粉与足量Cl2反应时转移的电子数为NA |