��Ŀ����
��2mol H2��1mol CO2�������Ϊ10L�ĺ����ܱ������У���һ�������·�����Ӧ��
��CO2(g) + H2(g) CO(g) + H2O(g)??????? ��H1����41.2kJ��moL��1��
CO(g) + H2O(g)??????? ��H1����41.2kJ��moL��1��
��CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ? ��H2����49kJ��moL��1��
CH3OH(g) + H2O(g) ? ��H2����49kJ��moL��1��
��Ӧ100min��ﵽƽ�⣬����±����ݣ�
�¶� | ת���ʣ�%�� | ���ʵ�����mol�� | ||
H2 | CO2 | CH3OH | CO | |
240�� |
| 10 | 0.05 | 0.05 |
����˵����ȷ����
A�������¶ȣ���Ӧ����ƽ�ⳣ����С
B�������¶ȣ�CH3OH�ĺ������
C��H2ת����Ϊ10%
D��100min�ڣ���Ӧ��������Ϊv(CO2)��0.0001 mol��L��1��min��1
C
��������
���������A����Ӧ��Ϊ���ȷ�Ӧ�����������¶ȣ���Ӧ����ƽ�ⳣ��������B����Ӧ��Ϊ���ȷ�Ӧ�������¶ȣ���Ӧ��ƽ�������ƶ���CH3OH�ĺ������٣�����C��CO2(g) + H2(g) CO(g) + H2O(g)����Ӧ��ת����H2Ϊ��n��H2��=n��CO��=0.05mol��CO2(g) + 3H2(g)
CO(g) + H2O(g)����Ӧ��ת����H2Ϊ��n��H2��=n��CO��=0.05mol��CO2(g) + 3H2(g) CH3OH(g) + H2O(g)����Ӧ��ת����H2Ϊ��n��H2��=3n��CH3OH��=3��0.05mol=0.15mol������H2ת����Ϊ����0.05mol+0.15mol����2mol��100%=10%����ȷ��D��100min�ڣ���Ӧ��������Ϊv(CO2)��v(CH3OH)= 0.05mol��10L��10min=0.0005 mol��L��1��min��1������
CH3OH(g) + H2O(g)����Ӧ��ת����H2Ϊ��n��H2��=3n��CH3OH��=3��0.05mol=0.15mol������H2ת����Ϊ����0.05mol+0.15mol����2mol��100%=10%����ȷ��D��100min�ڣ���Ӧ��������Ϊv(CO2)��v(CH3OH)= 0.05mol��10L��10min=0.0005 mol��L��1��min��1������
���㣺���⿼�黯ѧ��Ӧ���ʡ�ת���ʺͻ�ѧƽ��ļ��㡣

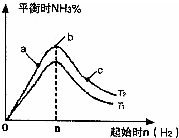 ����N2��H2����ʵ��NH3�Ĺ�ҵ�ϳɣ������ֿ��Խ�һ���Ʊ����ᣬ�ڹ�ҵ��һ��ɽ���������������ش��������⣺
����N2��H2����ʵ��NH3�Ĺ�ҵ�ϳɣ������ֿ��Խ�һ���Ʊ����ᣬ�ڹ�ҵ��һ��ɽ���������������ش��������⣺ 2NH3��g������H=-92.4kJ/mol
2NH3��g������H=-92.4kJ/mol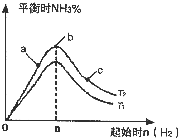 ����N2��H2����ʵ��NH3�Ĺ�ҵ�ϳɣ������ֿ��Խ�һ���Ʊ����ᣬ�ڹ�ҵ��һ��ɽ���������������ش��������⣺
����N2��H2����ʵ��NH3�Ĺ�ҵ�ϳɣ������ֿ��Խ�һ���Ʊ����ᣬ�ڹ�ҵ��һ��ɽ���������������ش��������⣺ )
) 2NH3(g) ��H=��92.4kJ/mol
2NH3(g) ��H=��92.4kJ/mol