题目内容
14.下列说法合理的是( )| A. | 液态氟化氢中存在氢键,所以其分子比氯化氢更稳定 | |
| B. | 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S | |
| C. | 邻羟基苯甲醛沸点高于对羟基苯甲醛是因为形成了分子内氢键 | |
| D. | 若X+和Y2-的核外电子层结构相同,则原子序数:Y<X |
分析 A.氢化物的稳定性与非金属的非金属性强弱有关,与氢键无关;
B.元素最高价氧化物对应水化物的酸性越强,则非金属性越强;
C.邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛能够形成分子间氢键,分子内氢键要弱于分子间氢键;
D.若X+和Y2-的核外电子层结构相同,则X位于Y的下一个周期.
解答 解:A.氢化物的稳定性与非金属的非金属性强弱有关,与氢键无关,氢键影响氢化物的熔沸点,故A错误;
B.比较最高价氧化物对应水化物的酸性,才能比较非金属性,故B错误;
C、由于邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛能够形成分子间氢键,而分子内氢键要弱于分子间氢键,所以邻羟基苯甲醛比对羟基苯甲醛熔、沸点低,故C错误;
D.若X+和Y2-的核外电子层结构相同,电X位于Y的下一个周期,故原子序数Y<X,故D正确;
故选D.
点评 本题考查非金属元素性质的递变规律,为高频考点,题目难度中等,明确元素周期表结构、原子结构及元素周期律的关系是解本题关键,易错选项是A,注意氢键只影响氢化物的熔沸点,化学键影响物质稳定性,注意二者的区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.下列装置或操作不能达到实验目的是( )
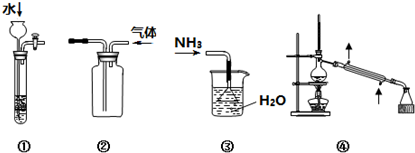

| A. | 装置①关闭活塞,往长颈漏斗中加水,可用于检查该装置的气密性 | |
| B. | 装置②可用于收集NH3、H2等 | |
| C. | 装置③可用于吸收NH3 | |
| D. | 装置④蒸馏时,冷却水从下口进、上口出 |
2.下列说法正确的是( )
| A. | C60、石墨和金刚石属于同素异形体 | |
| B. | 氯水、氨水、王水是混合物,水银、水玻璃是纯净物 | |
| C. | CO2、Cl2、CH3CH2OH是非电解质 | |
| D. | Al2O3可作为耐高温坩埚的材料,该材质的坩埚可用于加热NaOH固体 |
9.下列反应的离子方程式正确的是( )
| A. | 将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 金属钠加入水中:2Na+2H+═2Na++H2↑ | |
| C. | 铜与硝酸银溶液反应:Cu+2Ag+═Cu2++2Ag | |
| D. | 碳酸氢钙溶于盐酸中:CO32-+2H+═CO2↑+H2O |
6.下列说法错误的是( )
| A. | 可用 CuSO4溶液除去乙炔中的硫化氢杂质气体 | |
| B. | 煤焦油中含有苯、二甲苯等化工原料 | |
| C. | 天然气和可燃冰的主要成分都是甲烷 | |
| D. | 石油裂解的主要目的是为了得到更多的汽油 |
3.镁、铝混合粉末10.2g溶于500mL 4mol•L-1盐酸中.若加入2mol•L-1的氢氧化钠溶液,使得沉淀达到最大量,则需加入氢氧化钠溶液的体积为( )
| A. | 100 mL | B. | 500 mL | C. | 1 000 mL | D. | 1 500 mL |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA | |
| B. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 相同质量的N2和CO所含有的分子数、原子总数、电子总数都相等 | |
| D. | 1 mol CH5+中含有的电子数目为11NA |
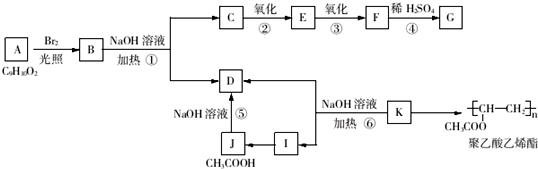
 .
.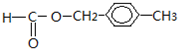 .
.