题目内容
17.将一定量的SO2通入FeCl3溶液中,取混合溶液,分别进行下列实验,其中能够证明SO2与FeCl3溶液发生氧化还原反应的是( )| 操作 | 现象 | |
| A | 加入NaOH溶液 | 有红褐色沉淀 |
| B | 加入酸化的Ba(NO3)2溶液 | 有白色沉淀 |
| C | 加入酸性KMnO4溶液 | 紫色褪去 |
| D | 加入KSCN溶液 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
分析 SO2与FeCl3溶液发生氧化还原反应,则生成硫酸和亚铁离子,酸性条件下,二氧化硫、亚铁离子可被硝酸根离子、高锰酸钾氧化,与KSCN不反应,以此解答该题.
解答 解:A.加入氢氧化钠生成红褐色沉淀,说明生成氢氧化铁,不能说明SO2与FeCl3溶液发生氧化还原反应,故A错误;
B.酸性条件下硝酸根离子也可氧化二氧化硫,可生成硫酸钡沉淀,不能说明SO2与FeCl3溶液发生氧化还原反应,故B错误;
C.加入酸性KMnO4溶液,紫色退去,因为二氧化硫具有还原性能够还原酸性高锰酸钾,即使二氧化硫与三价铁离子不发生氧化还原反应,也可使其溶液褪色,所以不能证明SO2与FeCl3溶液发生氧化还原反应,故C错误;
D.加入KSCN溶液,无明显现象,说明不存在铁离子,可说明SO2与FeCl3溶液发生氧化还原反应,故D正确.
故选D.
点评 本题考查了含二氧化硫与氯化铁性质及综合应用,题目难度中等,涉及氧化还原反应以及实验的评价等知识,充分考查学生的分析能力及灵活应用能力,注意熟练掌握含硫物质性质及应用方法.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
7.化学与生活密切相关,下列有关说法错误的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 食用油反复加热不会产生稠环芳香烃等有害物质 | |
| C. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| D. | 医用消毒酒精中乙醇的浓度为75% |
8.下列关于钠及其化合物的说法错误的是( )
| A. | 钠着火时可用细砂来灭火 | |
| B. | 切开的金属钠暴露在空气中,光亮的表面变暗发生2Na+O2═Na2O2反应 | |
| C. | 过氧化钠在潮湿空气放一段时间变成白色粘稠物的反应主要是:2Na2O2+2H2O═4NaOH+O2↑ | |
| D. | 过氧化钠投入硫酸铜溶液可产生氢氧化铜沉淀和氧气 |
5.在一定温度下的某容积不变的密闭容器中,建立下列化学平衡C(s)+H2O(g)?CO(g)+H2(g),不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | v正(H2O)=v正(H2) | |
| B. | V正(CO)=V逆(H2O) | |
| C. | 生成nmolCO的同时生成nmolH2O | |
| D. | 1 molH-H键断裂的同时断裂2molH-O键 |
12.下列表示对应化学反应的离子方程式正确的是( )
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O=HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2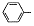 +CO2+H2O→2 +CO2+H2O→2 OH+CO32- OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
2.用NA表示阿伏加德罗常数的数值.下列叙述正确的是( )
| A. | 6.4 g SO2与足量氧气反应生成SO3时,转移的电子数为0.2NA | |
| B. | 1 mol氯气与足量FeI2溶液反应时,转移的电子数为2NA | |
| C. | 标准状况下,5.6 L NO和5.6 LO2混合后的气体中含有的分子数为0.5NA | |
| D. | 50 mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2的分子数为0.46NA |
9.我国高速铁路技术世界领先.高速铁路的无缝钢轨是将钢轨间的接头用铝与氧化铁发生铝热反应进行焊接而成的.对于铝热反应:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,下列说法中正确的是( )
| A. | Fe元素的化合价升高 | B. | Al化合价升高 | ||
| C. | 该反应是化合反应 | D. | Al化合价没变 |
10.下列叙述正确的是( )
| A. | 碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱 | |
| B. | 石英、水晶、硅石的主要成分都是二氧化硅 | |
| C. | 二氧化硅的化学性质活泼,能与任意的酸、碱发生反应 | |
| D. | 碳族元素的单质都有导电性 |