题目内容
9.我国高速铁路技术世界领先.高速铁路的无缝钢轨是将钢轨间的接头用铝与氧化铁发生铝热反应进行焊接而成的.对于铝热反应:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,下列说法中正确的是( )| A. | Fe元素的化合价升高 | B. | Al化合价升高 | ||
| C. | 该反应是化合反应 | D. | Al化合价没变 |
分析 反应Fe2O3+2Al $\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3中,Fe元素化合价由+3价降低到0价,被还原,Fe2O3为氧化剂,Al元素化合价由0价升高到+3价,被氧化,Al为还原剂,以此解答该题.
解答 解:由反应的方程式可知,Fe元素化合价由+3价降低到0价,被还原,发生还原反应,Al元素化合价由0价升高到+3价,化合价升高,被氧化,Al为还原剂,该反应是置换反应,故选B.
点评 本题考查氧化还原反应,为高频考点,侧重于学生的分析能力的考查,注意从元素化合价的角度认识相关概念以及物质的性质,难度不大.

练习册系列答案
相关题目
16.在标准状况下,1LN2中含m个氮分子,则阿伏加德罗常数可表示为( )
| A. | m/mol | B. | m/mol | C. | 22.4m | D. | 22.4m/mol |
17.将一定量的SO2通入FeCl3溶液中,取混合溶液,分别进行下列实验,其中能够证明SO2与FeCl3溶液发生氧化还原反应的是( )
| 操作 | 现象 | |
| A | 加入NaOH溶液 | 有红褐色沉淀 |
| B | 加入酸化的Ba(NO3)2溶液 | 有白色沉淀 |
| C | 加入酸性KMnO4溶液 | 紫色褪去 |
| D | 加入KSCN溶液 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
14.有关反应“H-+NH3═H2+NH2-”的说法正确的是( )
| A. | 该反应属于置换反应 | |
| B. | NH3是氧化剂 | |
| C. | H-、NH3的总能量与H2、NH2-的总能量之差为该反应的活化能 | |
| D. | 若反应中有1mol电子转移,则生成1g H2 |
14.根据下列实验事实得出的相应结论正确的是( )
| 实验事实 | 结论 | |
| A | NH3的水溶液可以导电 | NH3是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | Ca(ClO)2溶液中通入CO2产生白色沉淀 | 酸性:H2CO3>HClO |
| D | 硝酸具有挥发性 | 硝酸不稳定 |
| A. | A | B. | B | C. | C | D. | D |
1.下列说法中正确的是( )
| A. | 1 mol氧含有6.02×l023个微粒 | |
| B. | 阿伏加德罗常数数值约等于6.02×l0 23 | |
| C. | 硫的摩尔质量等于它的相对原子质量 | |
| D. | CO2的摩尔质量为44g |
18.下列溶液中溶质的物质的量浓度为1mol/L的是( )
| A. | 将40 g NaOH固体溶于1 L水中 | |
| B. | 将22.4 L氯化氢气体溶于水配成1L溶液 | |
| C. | 将1L 10mol/L的浓盐酸与9L水混合 | |
| D. | 将10g NaOH固体溶解在水中配成250 mL溶液 |
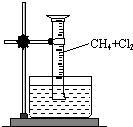 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.