题目内容
常温下,向Na2CO3溶液中逐滴滴入0.1mol/L盐酸,溶液的pH随着滴入盐酸溶液体积变化曲线如下图,则下列说法正确的是

A.a点时溶液pH=11.5,原因是:CO32-+2H2O → H2CO3+2OH-
B.a-b段发生反应为:CO32-+2H+→ CO2↑+H2O
C.b-c段发生反应为:HCO3-+H+→ CO2↑+H2O
D.c-d段发生反应为:H++OH-→ H2O
C
【解析】
试题分析:A.碳酸钠是强碱弱酸盐,碳酸根水解溶液显碱性,但碳酸根水解分步进行,则a点时溶液pH=11.5的原因是CO32-+H2O→HCO3-+OH-,A错误;B.碳酸钠与盐酸反应首先转化为碳酸氢钠,则根据图像可知a-b段发生反应为:CO32-+H+→HCO3-,B错误;C.产生的碳酸氢钠继续与盐酸反应放出CO2,所以b-c段发生反应为:HCO3-+H+→ CO2↑+H2O,C正确;D.根据图像可知c-d段盐酸过量,碳酸氢钠已经完全被消耗,D错误,答案选C。
考点:考查碳酸钠与盐酸反应的有关图像分析

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案(10分)氨有着广泛的用途,如可用于化肥、硝酸、合成纤维等工业生产。常用电离常数Kb和电离度α来定量表示氨水的电离程度,它们均可通过各浓度氨水对应的c(OH-)进行换算。下面是某中学化学兴趣小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
【仪器与试剂】酸度计、50 mL碱式滴定管、100mL烧杯、 0.10 mol·L-1 氨水
【实验数据】(不必填表格)
烧杯号 | V氨水 (mL) | V水(mL) | c (NH3·H2O) (mol·L-1) | c(OH-) | Kb | α |
1 | 50.00 | 0.00 | 1.34×10-3 | |||
2 | 25.00 | 25.00 | 9.48×10-4 | |||
3 | 5.00 | 45.00 | 4.24×10-4 |
请根据以上信息回答下述问题:
(1)25℃时,氨水的电离常数:Kb 。
。
(2)用0.10mol·L—1盐酸分别滴定20.00mL0.10mol·L—1
的NaOH溶液和20.00mL0.10mol·L—1氨水所得的滴定曲线如图。
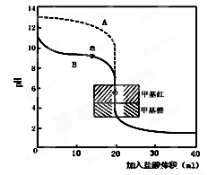
请指出盐酸滴定氨水的曲线为 (填A或B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序 。
(3)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有:
4NH3(g)+3O2(g)= 2N2(g)+6H2O(l) △H1 ①
4NH3(g)+5O2(g)= 4NO(g)+6H2O(l) △H2 ②
4NH3(g)+6NO(g)= 5N2(g)+6H2O(l) △H3 ③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= 。
(4)Allis-Chalmers制造公司发现可以用氨作为燃料电池的燃料。其总反应式为4NH3+3O2= 2N2+6H2O,正极上的电极反应式为O2+2H2O+4e—=4OH—,则负极上的电极反应式为 。
(本题共12分)葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→ (C6H11O7)2 Ca (葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
实验流程如下:
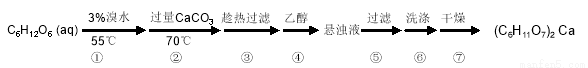
请回答下列问题:
32.第②步中所加CaCO3还发生了其他反应,写出其中一个主要反应的方程式________;充分反应后CaCO3固体需有剩余,目的是______________________;
33.第③步需趁热过滤,原因是______________________;
34.第④步加入乙醇的作用是______________________;
35.第⑥步中,下列洗涤剂最合适的是________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
锌是人体健康所必需的元素,葡萄糖酸锌是一种常用的补锌剂,对婴儿及青少年的智力和身体发育有重要作用。工业上以葡萄糖酸钙为原料通过如下两步制备葡萄糖酸锌:

步骤1:充分反应后,过滤除去CaSO4沉淀。步骤2:将葡萄糖酸溶液与ZnO混合。
36.步骤2中,待其充分反应后,须继续加入葡萄糖酸溶液至pH为5.8,目的是 。
37.下列物质可替代ZnO的是 (填字母)。
a.NH3·H2O
b.Zn(OH)2
c.NaOH
d.ZnSO4
e.ZnCO3

