题目内容
6.已知锶的核电核数为38,其单质密度为2.50g/cm3,下列说法中一定错误的是( )| A. | 颗粒状的单质锶与稀硫酸反应,反应现象不如钠和水反应剧烈 | |
| B. | 锶在纯净氮气中可以燃烧,燃烧产物投入水中可以放出气体 | |
| C. | 锶在纯氧中点燃可燃烧,燃烧生产的产物投入水中可以放出气体 | |
| D. | 颗粒状的单质锶投入水中,剧烈反应,生成大量的气体并引起气体燃烧和轻微爆炸 |
分析 第ⅡA族元素有铍、镁、钙、锶、钡、镭,同主族元素从上到下金属性逐渐增强,金属性越强,其单质与水反应越剧烈,其最高价氧化物的水化物的碱性越强;锶在纯净氮气中可以燃烧生成氮化锶,氮化锶与水反应生成氨气,据此分析.
解答 解:A.金属的活泼性:Sr>Ca>Na,则颗粒状锶单质与稀硫酸反应,反应现象比钠与水反应剧烈,故A错误;
B.锶在纯净氮气中可以燃烧生成氮化锶,氮化锶与水反应生成氨气,所以锶在氮气中燃烧产物与水反应可以放出气体,故B正确;
C.锶的最高价氧化物的水化物为强碱,则锶在纯氧中可以燃烧,燃烧产物与水反应生成的氢氧化物为强碱和氧气,故C正确;
D.锶的活泼性大于钙,所以与水反应更剧烈,则将颗粒状锶单质放入水中,反应剧烈,生成大量的气体,气体燃烧且发生轻微爆炸,故D正确;
故选A.
点评 本题考查了元素周期律,侧重于同主族元素性质的考查,注意把握同主族元素性质的变化规律,题目难度不大.

练习册系列答案
相关题目
12.某两种气态烃组成的混合物,取其2.24L(标准状况下)充分燃烧,得到0.16mol二氧化碳气体和3.6g液态水.据此判断下列分析中不正确的是( )
| A. | 此混合气体中可能含有乙烷 | |
| B. | 此气体中一定含有甲烷 | |
| C. | 此混合气体中一定不含有丙烷 | |
| D. | 此气体若是乙烯与甲烷的混合气体,则甲烷与乙烯的体积比为2:3 |
17.下列分子中,属于非极性分子的是( )
| A. | SO2 | B. | BeCl2 | C. | CH3Cl | D. | COCl2 |
14.“吃得营养,吃出健康”.以下说法正确的是( )
| A. | 油脂会使人发胖,故禁止食用 | B. | 霉变大米洗净后继续食用 | ||
| C. | 吃水果、蔬菜可以补充维生素 | D. | 食用加铁酱油预防甲状腺肿大 |
11.化学与科学技术、社会生活、环堍材料等密切相关.下列有关说法中错误的是( )
| A. | SO2是很好的抑菌剂,红酒中常加人微量的SO2 | |
| B. | 麦片中常加人微量铁粉,可以防止被氧化而变质 | |
| C. | “PM2.5“是指大气中直径≤2.5微米的颗粒物.其悬浮在空气中一定形成气溶胶 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
18.下列说法中,不正确的是( )
| A. | 干冰升华,克服的是CO2的分子间作用力 | |
| B. | 碳原子间连接方式的多样性,是含碳化合物种类繁多的原因之一 | |
| C. | 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成 | |
| D. | NH4Cl属于离子化合物,该物质中存在离子键和共价键 |
15.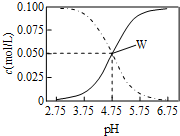 25℃时,在醋酸和醋酸钠混合溶液中有c(CH3COOH)+c(CH3COO-)=0.1mol/L且c(CH3COOH)、c(CH3COO-)与pH的关系如图.有关离子浓度叙述正确的是( )
25℃时,在醋酸和醋酸钠混合溶液中有c(CH3COOH)+c(CH3COO-)=0.1mol/L且c(CH3COOH)、c(CH3COO-)与pH的关系如图.有关离子浓度叙述正确的是( )
 25℃时,在醋酸和醋酸钠混合溶液中有c(CH3COOH)+c(CH3COO-)=0.1mol/L且c(CH3COOH)、c(CH3COO-)与pH的关系如图.有关离子浓度叙述正确的是( )
25℃时,在醋酸和醋酸钠混合溶液中有c(CH3COOH)+c(CH3COO-)=0.1mol/L且c(CH3COOH)、c(CH3COO-)与pH的关系如图.有关离子浓度叙述正确的是( )| A. | pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol/L | |
| B. | pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| C. | W点表示溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| D. | 向W点所表示溶液中通入0.05mol HCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) |
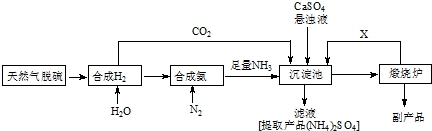
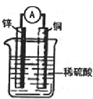 如图为某原电池示意图,请回答下列问题,
如图为某原电池示意图,请回答下列问题,