题目内容
20.下列有机物可在厨房中作调味剂的是( )| A. | 甘油 | B. | 醋酸 | C. | 淀粉 | D. | 汽油 |
分析 厨房中的调味剂常见的有:食醋、酱油、食盐、味精、料酒、糖等,据此分析.
解答 解:A、甘油是丙三醇,不能直接食用,故不能做调味剂,故A错误;
B、醋酸是食醋的主要成分,可以做调味剂,故B正确;
C、淀粉属于糖类,是基本营养物质,不是调味剂,故C错误;
D、汽油不能食用,不是调味剂,故D错误.
故选B.
点评 本题考查了化学物质在生活中的应用,难度不大,注意生活常识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列叙述正确的是( )
| A. | 汽油、柴油和植物油都属于烃 | |
| B. | 淀粉可水解生成葡萄糖,蔗糖可水解生成葡萄糖和果糖 | |
| C. | 苯和溴水在Fe3+催化下发生取代反应生成溴苯 | |
| D. | 硫酸铜溶液和食盐溶液均可使蛋白质溶液变性 |
8.下列关于油脂的说法正确的是( )
| A. | 甘油是油脂的一种 | |
| B. | 油脂中均含有酯基 | |
| C. | 油脂不能发生取代反应 | |
| D. | 油脂在酸性条件下的水解程度比碱性条件下大 |
15.在常温常压下,取下列四种有机物个1mol分别在足量的氧气中燃烧,消耗氧气最多的是( )
| A. | CH4 | B. | C2H5OH | C. | C3H8O | D. | C3H8O2 |
5.某烃的一种同分异构体,一氯代产物只有一种,则该烃的分子式可能为( )
| A. | C6H14 | B. | C7H16 | C. | C8H18 | D. | C9H20 |
20.近年来,我国在超导体材料研究方面居于世界领先地位,铊(Tl)是超导体的组成成分之一,铊位于第6周期ⅢA族.下列对铊的性质的推导不正确的是( )
| A. | 是易导电的银白色金属 | B. | Tl(OH)3是两性氢氧化物 | ||
| C. | Tl3+能形成+3价的化合物 | D. | 单质能与稀硝酸反应生成硝酸盐 |
1.X、Y、Z、R、M是元素周期表中原子序数依次增大的五种短周期元素,其相关信息如下表:
(1)Y、Z、R的第一电离能从大到小的顺序是N>O>C(填元素符号)
(2)Z、R的最简单氢化物中稳定性强的是H2O,沸点高的是H2O(填化学式)
(3)甲是由上述3种元素组成的常见化合物,常温下pH=3的甲溶液中由水电离c(H+)=10-3mol/L,则甲的化学式是NH4NO3.
(4)直线型分子Y2Z2中所有原子都达到8电子稳定结构,则分子中σ键与π键的个数之比是3:4.
(5)常温下0.58gY4H10完全燃烧放出29kJ的热量,请写出Y4H10燃烧热的热化学方程式C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2900kJ/mol.
| 元素 | 相关信息 |
| X | X的一种核素的原子核中没有中子 |
| Y | Y原子的核外电子占据4个原子轨道 |
| Z | Z的气态氢化物能使湿润的红色石蕊试纸变蓝 |
| R | R是地壳中含量最高的元素 |
| M | M的单质与冷水剧烈反应,生成的强碱中含有电子数相同的阴阳离子 |
(2)Z、R的最简单氢化物中稳定性强的是H2O,沸点高的是H2O(填化学式)
(3)甲是由上述3种元素组成的常见化合物,常温下pH=3的甲溶液中由水电离c(H+)=10-3mol/L,则甲的化学式是NH4NO3.
(4)直线型分子Y2Z2中所有原子都达到8电子稳定结构,则分子中σ键与π键的个数之比是3:4.
(5)常温下0.58gY4H10完全燃烧放出29kJ的热量,请写出Y4H10燃烧热的热化学方程式C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2900kJ/mol.
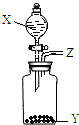 长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体.甲、乙两位同学发现往水中投入过氧化钙时产生气泡.
长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体.甲、乙两位同学发现往水中投入过氧化钙时产生气泡.