题目内容
4.相同温度下,等物质的量浓度的下列溶液中,pH最大的是( )| A. | Na2CO3 | B. | NaCl | C. | NH4Cl | D. | CH3COONa |
分析 根据盐的水解规律:有弱才水解,无弱不水解,谁强显谁性,越弱越水解来分析.
解答 解:NaCl是强酸强碱盐,不水解,溶液显中性,即pH=7,NH4Cl是强酸强碱盐,铵根离子水解溶液显酸性,PH<7,CH3COONa、Na2CO3均为强碱弱酸盐,均水解显碱性,但由于其对应的酸的酸性强弱关系为:CH3COOH>H2CO3,故当浓度相等时,水解程度为:Na2CO3>CH3COONa>7,即溶液pH最大的是Na2CO3,故选A.
点评 本题考查盐的水解.相同温度下,物质的量浓度相同的盐溶液,盐的组成中酸根离子对应的酸越弱,盐溶液中酸根离子水解程度越大,溶液pH越大,题目难度不大.

练习册系列答案
相关题目
12.下列各组粒子在指定的溶液中能大量共存的是( )
| A. | 加入铝片能放出氢气的溶液:Na+、CO32-、NO3-、NH4+ | |
| B. | 滴入酚酞显红色的溶液:CO32-、Na+、AlO2-、NO3- | |
| C. | 能使蓝色石蕊试纸变红的溶液:Na+、Cl-、S2-、ClO- | |
| D. | 滴入甲基橙显红色的溶液:MnO4-、K+、SO42-、CH3CH2OH |
9.将agFe2O3、Al2O3样品溶解在过量的200mL浓度为0.1mol•L-1的盐酸溶液中,然后向其中加入NaOH溶液,使Al3+、Fe3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
| A. | 0.1 mol/L | B. | 0.2 mol/L | C. | 0.4 mol/L | D. | 0.6mol/L |
13.有FeO、Fe2O3的混合物若干克,在CO气流中加热充分反应,冷却后称剩余固体比原混合物质量减轻0.8g,若将同质量的混合物与盐酸反应,欲使其完全溶解需1mol/L 的盐酸的体积为( )
| A. | 100mL | B. | 200mL | C. | 250mL | D. | 无法计算 |
14.下列表示正确的是( )
| A. | CH4的球棍模型示意图为 | B. | H2O2的电子式: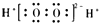 | ||
| C. | 葡萄糖的最简式为CH2O | D. | 聚丙烯的结构简式: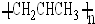 |

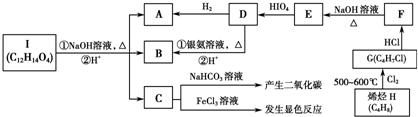
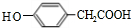 ,E
,E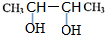 ;
; ;
;