题目内容
下表是元素周期表的一部分,表中的每个字母代表一种短周期元素,回答下列问题:

(1)画出A的原子结构示意图 .
(2)A、B、E、F、G形成的气态氢化物中最稳定的是 (填化学式).
(3)D在元素周期表中的位置是第3周期 族.
(4)E、F的最高价氧化物对应水化物的酸性,较强的是 (用化学式表示).

(1)画出A的原子结构示意图
(2)A、B、E、F、G形成的气态氢化物中最稳定的是
(3)D在元素周期表中的位置是第3周期
(4)E、F的最高价氧化物对应水化物的酸性,较强的是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表中的位置知,A、B、C、D、E、F、G分别是O、F、Na、Al、P、S、Cl元素,
(1)A原子核外有2个电子层、最外层有6个电子,据此画出原子结构示意图;
(2)同一周期元素,元素的非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱,元素的非金属性越强,其气态氢化物越稳定;
(3)主族元素中,原子电子层数与其周期数相等,最外层电子数与其族序数相等;
(4)同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强.
(1)A原子核外有2个电子层、最外层有6个电子,据此画出原子结构示意图;
(2)同一周期元素,元素的非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱,元素的非金属性越强,其气态氢化物越稳定;
(3)主族元素中,原子电子层数与其周期数相等,最外层电子数与其族序数相等;
(4)同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强.
解答:
解:根据元素在周期表中的位置知,A、B、C、D、E、F、G分别是O、F、Na、Al、P、S、Cl元素,
(1)A原子核外有2个电子层、最外层有6个电子,其原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)同一周期元素,元素的非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱,元素的非金属性越强,其气态氢化物越稳定,这几种元素中非金属性最强的是F元素,则气态氢化物稳定性最强的是HF,故答案为:HF;
(3)主族元素中,原子电子层数与其周期数相等,最外层电子数与其族序数相等,D元素是Al元素,Al原子核外有3个电子层、最外层电子数是3,所以D位于第三周期第IIIA族,故答案为:ⅢA;
(4)同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,E的非金属性小于F,所以E、F元素的最高价氧化物对应水化物的酸性较强的是H2SO4,故答案为:H2SO4.
(1)A原子核外有2个电子层、最外层有6个电子,其原子结构示意图为
 ,故答案为:
,故答案为: ;
;(2)同一周期元素,元素的非金属性随着原子序数增大而增强,同一主族元素,元素非金属性随着原子序数增大而减弱,元素的非金属性越强,其气态氢化物越稳定,这几种元素中非金属性最强的是F元素,则气态氢化物稳定性最强的是HF,故答案为:HF;
(3)主族元素中,原子电子层数与其周期数相等,最外层电子数与其族序数相等,D元素是Al元素,Al原子核外有3个电子层、最外层电子数是3,所以D位于第三周期第IIIA族,故答案为:ⅢA;
(4)同一周期元素,元素的非金属性随着原子序数增大而增强,元素的非金属性越强,其最高价氧化物的水化物酸性越强,E的非金属性小于F,所以E、F元素的最高价氧化物对应水化物的酸性较强的是H2SO4,故答案为:H2SO4.
点评:本题综合考查元素位构性的关系,侧重考查学生对化学用语、基本理论的运用,熟练掌握并灵活运用同一周期、同一主族的元素周期律,题目难度不大.

练习册系列答案
相关题目
设NA 为阿伏加德罗常数的值,下列叙述正确的是( )
| A、88.0g 干冰中含有的电子数为8.0NA |
| B、常温下,11.2 L 乙烯在氧气中完全燃烧转移的电子数为6.0NA |
| C、常温下1.0 L 0.1 mol?L-1NH4Cl 溶液中,NH4+和H+总数大于0.1NA |
| D、1.2g 金刚石中含有的碳碳键数为0.4 NA |
下列不能达到实验目的是( )
| A、等量的CH4和Cl2在光照下反应生成纯净的CH3Cl |
| B、将苯与浓硝酸和浓硫酸共热制取硝基苯 |
| C、将红热的铜丝迅速插入无水乙醇中可将乙醇氧化为乙醛 |
| D、可用浓硝酸鉴别淀粉溶液和鸡蛋白溶液 |
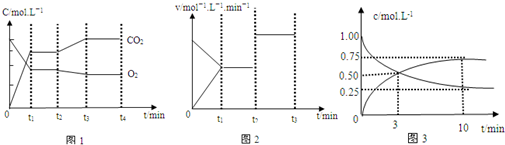
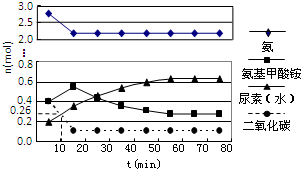 尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步:
尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步: 某小组学生想研究不同物质对双氧水分解速率的影响,以生成气体量50mL为标准,设计了如下实验方案:
某小组学生想研究不同物质对双氧水分解速率的影响,以生成气体量50mL为标准,设计了如下实验方案: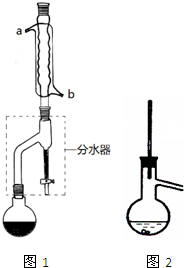 乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室制备乙酸正丁酯的化学方程式为:
乙酸正丁酯常用作织物、人造革和塑料生产过程中的溶剂,石油和医药工业中的萃取剂,也用于香料复配以及香蕉、菠萝、杏、梨等多种香味剂的成分.实验室制备乙酸正丁酯的化学方程式为: