题目内容
红矾钠(重铬酸钾:Na2Cr2O7.2H2O)是重要的化工原料,工业上用铬铁矿(主要成分是FeO.Cr2O3)制备红矾钠的过程中会发生如下反应:4FeO.Cr2O3(S)+8Na2CO3+7O2?8Na2CrO4(s)+2Fe2O3(s)+8CO2
△H<0
(1)请写出上述反应的化学平衡常数表达式:K=
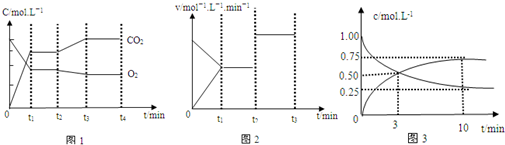
(2)如图1,图2表示上述反应在t2时达到平衡,在t2时因改变某个条件而发生变化的曲线.由图1判断反应进行至t2时,曲线发生变化的原因是 用文字表述);由图2判断,t2到t3的曲线变化的原因可能是 (填写序号)
a、升高温度 b、加了催化剂c、通入O2 d、缩小容器体积
(3)工业生可用上述反应的副产物CO2来生产甲醇,为测定反应速率,进行了如下实验,在体积为1L的密闭容
器中,充入1molCO2和3molH2,在500℃下发生反应:CO2(g)+3H2?CH3OH(g)+H2O(g)△H=-49.0kJ.mol-1测得CO2和CH3OH(g)的浓度随时间变化曲线如图3所示.从反应开始到建立平衡,二氧化碳的平均反应速率v(CO2)= .
△H<0
(1)请写出上述反应的化学平衡常数表达式:K=
(2)如图1,图2表示上述反应在t2时达到平衡,在t2时因改变某个条件而发生变化的曲线.由图1判断反应进行至t2时,曲线发生变化的原因是
a、升高温度 b、加了催化剂c、通入O2 d、缩小容器体积

(3)工业生可用上述反应的副产物CO2来生产甲醇,为测定反应速率,进行了如下实验,在体积为1L的密闭容
器中,充入1molCO2和3molH2,在500℃下发生反应:CO2(g)+3H2?CH3OH(g)+H2O(g)△H=-49.0kJ.mol-1测得CO2和CH3OH(g)的浓度随时间变化曲线如图3所示.从反应开始到建立平衡,二氧化碳的平均反应速率v(CO2)=
考点:化学平衡的计算,化学平衡的影响因素
专题:化学平衡专题
分析:(1)化学平衡常数K=
,固态和纯液体不列入;
(2)影响平衡移动的因素只有温度、浓度、压强,据图1可知,CO2浓度增大,O2浓度减小,说明平衡正向移动;图2中,t2到t3的曲线变化说明平衡没有移动,只是反应速率加快,据影响反应速率的因素和平衡移动的因素分析;
(3)根据图象中二氧化碳的变化来计算反应速率.
| 生成物平衡浓度幂次方乘积 |
| 反应物平衡浓度幂次方乘积 |
(2)影响平衡移动的因素只有温度、浓度、压强,据图1可知,CO2浓度增大,O2浓度减小,说明平衡正向移动;图2中,t2到t3的曲线变化说明平衡没有移动,只是反应速率加快,据影响反应速率的因素和平衡移动的因素分析;
(3)根据图象中二氧化碳的变化来计算反应速率.
解答:
解:(1)化学平衡常数K=
,反应4FeO?Cr2O3(s)+8Na2CO3(s)+7O2?8Na2CrO4(s)+2Fe2O3(s)+8CO2的平衡常数表达式为:K=
,故答案为:
;
(2)据图1可知,CO2浓度逐渐增大,O2浓度逐渐减小,说明平衡正向移动,正反应放热,只能是降温;图2中,t2到t3的曲线变化说明平衡没有移动,只是反应速率加快,升温平衡逆向移动,加入氧气平衡正向移动,缩小容器体积平衡逆向移动,只能是加入了催化剂;
故答案为:对平衡体系降温;b;
(3)图象可知,二氧化碳反应速率=
=0.075mol/L;
故答案为:0.075mol/L;
| 生成物平衡浓度幂次方乘积 |
| 反应物平衡浓度幂次方乘积 |
| c8(CO2) |
| c7(O2) |
| c8(CO2) |
| c7(O2) |
(2)据图1可知,CO2浓度逐渐增大,O2浓度逐渐减小,说明平衡正向移动,正反应放热,只能是降温;图2中,t2到t3的曲线变化说明平衡没有移动,只是反应速率加快,升温平衡逆向移动,加入氧气平衡正向移动,缩小容器体积平衡逆向移动,只能是加入了催化剂;
故答案为:对平衡体系降温;b;
(3)图象可知,二氧化碳反应速率=
| 1.0mol/L-0.25mol/L |
| 10min |
故答案为:0.075mol/L;
点评:本题结合图象考查了化学平衡常数表达式、影响平衡移动和化学反应速率的因素,题目难度中等,注意分析图象.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、玻璃钢是一种复合材料,由基体和增强体组成,基体起骨架作用 |
| B、SO2溶于水,其水溶液能导电,说明SO2是电解质 |
| C、食醋、纯碱、食盐分别属于酸、碱、盐 |
| D、生铁、不锈钢、青铜都属于合金 |
常温下,有物质的量浓度、体积都相同的NaA(pH=8)溶液和NaB(pH=12)溶液,下列说法中不正确的是( )
| A、NaA溶液中c(Na+)-c(A-)=10-6mol?L-1 |
| B、NaB溶液中c(H+)+c(HB)=10-2mol?L-1 |
| C、将两溶液混合,混合溶液中:c(OH-)>5×10-3mol?L-1 |
| D、两溶液中的离子总数不相等 |
下列叙述不正确的是( )
| A、油脂是多种高级脂肪酸的甘油酯,要合理摄入 |
| B、乙酸乙酯和高级脂肪酸甘油酯都能与氢氧化钠溶液发生反应,都有酸性 |
| C、植物油能使酸性高锰酸钾溶液褪色 |
| D、油脂的水解反应是取代反应 |
 滴定法是一种用于测定的非常重要的方法.
滴定法是一种用于测定的非常重要的方法.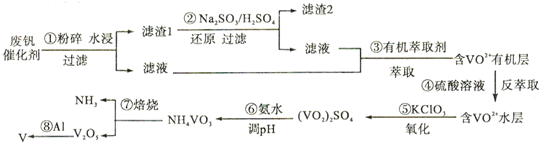




 如图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1mol.X、E、G的焰色反应均为黄色.回答下列问题:
如图表示的反应关系中,部分产物被略去.已知2mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B、无色气体C各1mol.X、E、G的焰色反应均为黄色.回答下列问题: