题目内容
下列物质的量浓度关系错误的是
| A.等物质的量浓度的HA溶液与MOH溶液等体积混合:c(H+)+c(M+)=c(OH-)+c(A-) |
| B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) |
| C.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合: c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
D.0.1 mol·L-1的NaHCO3溶液:c(Na+)>c(OH-)>c(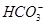 )>c(H+) )>c(H+) |
D
利用电荷守恒即可得出A项正确;由于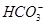 的酸性比CH3COOH的酸性弱,所以
的酸性比CH3COOH的酸性弱,所以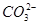 水解的程度大,其c(Na2CO3)<c(CH3COONa),而NaOH是电离出OH-,故B项正确;利用原子守恒2c(Na+)=c(CH3COO-)+c(CH3COOH)和电荷守恒c(CH3COO-)+c(OH-)=c(H+)+c(Na+)乘以2联立,消去c(Na+)即可得出c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),C项正确;D项
水解的程度大,其c(Na2CO3)<c(CH3COONa),而NaOH是电离出OH-,故B项正确;利用原子守恒2c(Na+)=c(CH3COO-)+c(CH3COOH)和电荷守恒c(CH3COO-)+c(OH-)=c(H+)+c(Na+)乘以2联立,消去c(Na+)即可得出c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),C项正确;D项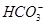 水解微弱,其浓度应该大于OH-的浓度,D项不正确。
水解微弱,其浓度应该大于OH-的浓度,D项不正确。
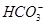 的酸性比CH3COOH的酸性弱,所以
的酸性比CH3COOH的酸性弱,所以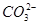 水解的程度大,其c(Na2CO3)<c(CH3COONa),而NaOH是电离出OH-,故B项正确;利用原子守恒2c(Na+)=c(CH3COO-)+c(CH3COOH)和电荷守恒c(CH3COO-)+c(OH-)=c(H+)+c(Na+)乘以2联立,消去c(Na+)即可得出c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),C项正确;D项
水解的程度大,其c(Na2CO3)<c(CH3COONa),而NaOH是电离出OH-,故B项正确;利用原子守恒2c(Na+)=c(CH3COO-)+c(CH3COOH)和电荷守恒c(CH3COO-)+c(OH-)=c(H+)+c(Na+)乘以2联立,消去c(Na+)即可得出c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),C项正确;D项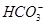 水解微弱,其浓度应该大于OH-的浓度,D项不正确。
水解微弱,其浓度应该大于OH-的浓度,D项不正确。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 )+c(H2CO3)
)+c(H2CO3) )+c(
)+c(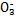 )>c(S
)>c(S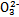 )>c(OH-)
)>c(OH-)