题目内容
下列说法正确的是
A.CO2的水溶液能导电,所以CO2是电解质
B.强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强
C.液溴不导电,所以溴是非电解质
D.BaSO4难溶于水,其水溶液的导电能力极弱,所以BaSO4是弱电解质
B
【解析】
试题分析:A、CO2的水溶液能导电是因为二氧化碳与水反应生成的碳酸电离出自由移动的氢离子和碳酸氢根,而不二氧化碳自身电离,所以碳酸是电解质,CO2是非电解质,错误;B、溶液导电性与溶液中离子浓度及离子所带电荷多少有关,与电解质的强弱无关,错误;C、液溴为单质,既不是电解质也不是非电解质,错误;D、BaSO4难溶于水,但溶解的部分完全电离,所以BaSO4是强电解质,错误。
考点:考查电解质的概念及溶液的导电性。

练习册系列答案
相关题目
下列实验不能达到预期目的的是
序号 | 实验操作 | 实验目的 |
A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
B | 用同一电路测定等浓度的盐酸、醋酸两溶液的导电性 | 比较盐酸、醋酸的相对强弱 |
C | 测定Na2CO3、Na2SO4两溶液的pH | 比较碳、硫的非金属性强弱 |
D | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
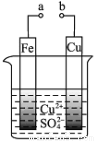
 。下列有关说法正确的是
。下列有关说法正确的是
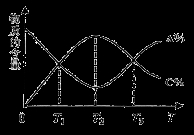
 cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是
cC(g)。反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是