题目内容
有关下图的说法正确的是
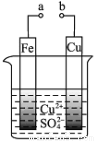
A.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+
B.构成原电池时溶液中SO42- 移向Cu极
C.要使Fe极不被腐蚀,Cu片换Zn片或a接直流电源负极
D.形成电解池,Cu电极不可能溶解
C
【解析】
试题分析:Cu2+移向正极,并且在正极上得到电子发生还原反应,析出单质铜覆盖在正极表面,即Cu2++2eˉ=Cu,故A错误; 构成原电池时,SO42-移向负极,带正电的Cu2+移向正极,故B错误;保护Fe极的方法就是使其作正极或阴极,可以与比Fe活泼的金属构成原电池,或者与直流电源的负极相连,故C正确;形成电解池,Cu电极为阳极,Cu电极可溶解, 故D错误;
考点:考查电化学基础,涉及原电池内电路中离子移动方向、电极反应式、金属的电化学腐蚀与防护、电解原理等知识。

练习册系列答案
相关题目
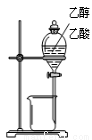
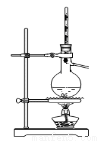
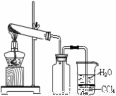
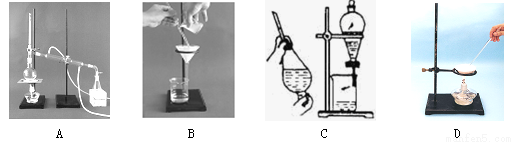
用下列实验装置完成对应的实验,不能达到实验目的的是
A | B | C | D | |
装置 |
|
|
|
|
实验 | 分离乙醇和乙酸 | 证明温度对化学平衡的影响 | 分离沸点相差较大的互溶液体混合物 | 制取并收集氨气 |
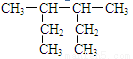 3-甲基-2-乙基戊烷
3-甲基-2-乙基戊烷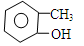 邻甲基苯酚
邻甲基苯酚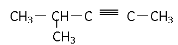 2-甲基-3-戊炔
2-甲基-3-戊炔