题目内容
下列关于物质的量浓度表述正确的是
A.0.3 mol·L-1的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.9 mol
B.1 L水吸收22.4 L氨气时所得氨水的浓度是1 mol·L-1
C.在K2SO4和NaCl的中性混合溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同
D.10 ℃时,100 mL 0.35 mol·L-1的KCl饱和溶液蒸发掉5 g水冷却到10 ℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol·L-1
D
【解析】
试题分析:A、缺少溶液的体积,无法计算0.3 mol·L-1的Na2SO4溶液中含有Na+和SO42-的总物质的量,错误;B、缺少温度和压强,无法确定22.4 L氨气的物质的量;根据C=n/V中,V指溶液的体积不是溶剂的体积,错误;C、在K2SO4和NaCl的中性混合溶液中,如果Na+和SO42—的物质的量相等,硫酸根离子所带电荷大于钠离子所带电荷,根据溶液中阴阳离子所带电荷相等,所以K+的物质的量浓度大于Cl-的物质的量浓度,错误;D、温度相同时,同一物质的饱和溶液中溶液的物质的量浓度一定相同,与溶液的体积无关,正确。
考点:考查物质的量浓度。

练习册系列答案
 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
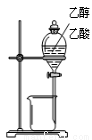
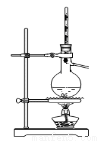
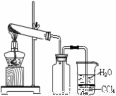
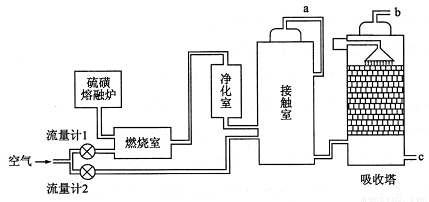
用下列实验装置完成对应的实验,不能达到实验目的的是
A | B | C | D | |
装置 |
|
|
|
|
实验 | 分离乙醇和乙酸 | 证明温度对化学平衡的影响 | 分离沸点相差较大的互溶液体混合物 | 制取并收集氨气 |


 可以表示羟基,也可以表示氢氧根离子
可以表示羟基,也可以表示氢氧根离子 可以表示二氧化碳分子,也可以表示水分子
可以表示二氧化碳分子,也可以表示水分子 的阴离子都不能破坏水的电离平衡
的阴离子都不能破坏水的电离平衡 可以表示12C,也可以表示14C
可以表示12C,也可以表示14C


 ,聚合物
,聚合物 可用于制备高吸水性树脂,其单体的结构简式为__________________。以CH3COOH和化合物I为原料可合成该单体,涉及的反应的化学方程式为_______________、_________________。
可用于制备高吸水性树脂,其单体的结构简式为__________________。以CH3COOH和化合物I为原料可合成该单体,涉及的反应的化学方程式为_______________、_________________。