题目内容
X、Y、Z、W为四种短周期主族元素,它们在周期表中的位置如右图所示。X的最高价氧化物和气态氢化物的分子都是由极性键形成的非极性分子。下列性质比较中正确的是

A.最高价氧化物的水化物的酸性:Y<X<W
B.离子半径由小到大的顺序:W<Z<Y
C.单质晶体的熔点由低到高的顺序:Y<W<Z
D.原子最外层的电子数:Z<Y<X
B
【解析】
试题分析:根据题意可确定:X是C,Y是N;Z是Na;W是Al。A.元素的非金属性越强,其最高价的氧化物对应的水化物的酸性就越强,由于元素的非金属性:Y>X>W,所以最高价氧化物的水化物的酸性:Y>X>W,错误;B.W、Z、Y形成的两种电子层结构相同。对于电子层结构相同的离子来说,核电荷数越大,离子的半径就越小。所以离子半径由小到大的顺序:W<Z<Y,正确;C.N2是分子晶体,分子间通过分子间作用力结合,而金属Na、Al是金属晶体,分子晶体的熔沸点比金属金属晶体的低,由于Al原子半径比Na小,金属键比Na强,所以熔沸点Al>Na,单质晶体的熔点由低到高的顺序:Y<Z <W,错误;D.原子最外层的电子数:Z<X <Y,错误。
考点:考查元素的推断、元素周期表、元素周期律的应用的知识。

练习册系列答案
相关题目

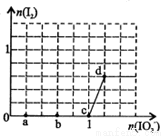
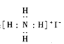

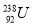
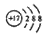
 2XY3(g) ΔH=—92.6KJ/mol
2XY3(g) ΔH=—92.6KJ/mol


 ,聚合物
,聚合物 可用于制备高吸水性树脂,其单体的结构简式为__________________。以CH3COOH和化合物I为原料可合成该单体,涉及的反应的化学方程式为_______________、_________________。
可用于制备高吸水性树脂,其单体的结构简式为__________________。以CH3COOH和化合物I为原料可合成该单体,涉及的反应的化学方程式为_______________、_________________。