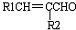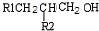题目内容
下列说法中,正确的是( )
| A、强电解质溶液一定比弱电解质溶液的导电性强 |
| B、强电解质的水溶液中不存在分子 |
| C、SO2和乙醇均属共价化合物,在水中都不能电离,均属非电解质 |
| D、不同的弱电解质只要物质的量浓度相同,电离程度也相同 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A.强弱电解质与溶液的导电性没有必然关系;
B.强电解质的水溶液中存在水分子;
C.SO2自身不能电离,是非电解质;乙醇在水中不能电离,是非电解质;
D.弱电解质部分电离,不同的弱电解质,其电离程度可能不同,无法比较其电离程度.
B.强电解质的水溶液中存在水分子;
C.SO2自身不能电离,是非电解质;乙醇在水中不能电离,是非电解质;
D.弱电解质部分电离,不同的弱电解质,其电离程度可能不同,无法比较其电离程度.
解答:
解:A.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关,强电解质溶液的导电能力不一定比弱电解质溶液强,故A错误;
B.强电解质溶于水的部分完全电离,但水是弱电解质,部分电离,故存在水分子,故B错误;
C.SO2自身不能电离,是非电解质;乙醇在水中不能电离,是非电解质,故C正确;
D.不同的弱电解质,电离程度可能不同,电离程度与物质的量浓度没有必然关系,故D错误;
故选C.
B.强电解质溶于水的部分完全电离,但水是弱电解质,部分电离,故存在水分子,故B错误;
C.SO2自身不能电离,是非电解质;乙醇在水中不能电离,是非电解质,故C正确;
D.不同的弱电解质,电离程度可能不同,电离程度与物质的量浓度没有必然关系,故D错误;
故选C.
点评:本题考查强弱电解质判断、溶液导电性影响因素、非电解质的判断,题目难度不大.注意掌握强弱电解质的概念及判断方法,明确溶液的导电性与强弱电解质没有必然关系.

练习册系列答案
相关题目
下列说法正确的是( )
①金属钠、氢气都能在氯气中燃烧,生成白色烟雾;
②铜丝在氯气中燃烧,生辰蓝绿色的氯化铜;
③点燃是使氯气跟氢气化合的唯一条件;
④氯气跟变价金属反应生成高价金属氯化物.
①金属钠、氢气都能在氯气中燃烧,生成白色烟雾;
②铜丝在氯气中燃烧,生辰蓝绿色的氯化铜;
③点燃是使氯气跟氢气化合的唯一条件;
④氯气跟变价金属反应生成高价金属氯化物.
| A、②③ | B、①② | C、①④ | D、④ |
我国镍氢电池居世界先进水平.常见镍氢电池的某极是储氢合金LaNi5H6 (LaNi5H6中各元素化合价均为零),电池反应通常表示为LaNi5H6+6NiO(OH)?LaNi5+6Ni(OH)2,下列说法正确的是( )
| A、放电时储氢合金作正极 |
| B、充电时阳极周围c(OH-)增大 |
| C、放电时负极反应:LaNi5H6+6OH--6e-=LaNi5+6H2O |
| D、充电时储氢合金作阳极 |
对于方程Al2O3+N2+3C=2AlN+3CO下列说法正确的是( )
| A、Al2O3做氧化剂 |
| B、N2是还原剂 |
| C、AlN既是氧化产物又是还原产物 |
| D、若有1mol CO生成,则反应中有2mol电子转移 |
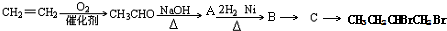
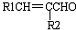 +H2O(-R1、R2表示氢原子或烃基)
+H2O(-R1、R2表示氢原子或烃基)