题目内容
向某烧碱溶液中通入5.28gCO2后,将溶液在低温下蒸干,得到固体物质的质量为17.32g,则该固体物质是( )
| A、Na2CO3 |
| B、NaHCO3 |
| C、Na2CO3和NaOH |
| D、Na2CO3和NaHCO3 |
考点:化学方程式的有关计算
专题:计算题
分析:盐与气体的质量相比,生成正盐比生成酸式盐质量增重多,若生成正盐,假设全为Na2CO3,生成的盐的质量最重,NaOH可能有剩余,故最大值可能大于盐的极大值,据此计算判断.
解答:
解:5.28gCO2物质的量是0.12mol,2NaOH+CO2=Na2CO3+H2O(如多所有CO2全部反应生成Na2CO3那么固体质量应为0.12mol×106g/mol=12.72g<17.32g,NaOH+H2O+CO2=NaHCO3,如所有CO2全部反应生成NaHCO3那么固体质量应为0.12mol×84g/mol=10.08g<17.32g,题目给的是“将溶液在低温下蒸干”所以不会分解,k可能会发生反应:NaOH+NaHCO3=Na2CO3+H2O,所以固体一定会有NaOH剩余,综上所述:则该固体物质有Na2CO3和和NaOH.
故选C.
故选C.
点评:本题考查混合物的有关计算,难度较大,关键是利用极值法进行解答,注意氢氧化钠可能会剩余.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
由两种元素形成的合金5.0克与足量的酸反应产生0.25摩尔的氢气,这种合金可能是( )
| A、Zn和Fe |
| B、Mg和Al |
| C、Fe和Si |
| D、Mg和Cu |
随着社会的发展,人们日益重视环境问题,下列做法或说法不正确的是( )
| A、对垃圾进行无害化、资源化处理 |
| B、将煤气化或液化,获得清洁燃料 |
| C、PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 |
| D、推广使用无磷洗衣粉和无氟冰箱 |
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确的是( )
A、ρ=
| ||
B、ω=
| ||
C、ω=
| ||
D、c=
|
 某有机物的结构式如图它在一定条件下可能发生的反应有①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥加聚( )
某有机物的结构式如图它在一定条件下可能发生的反应有①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥加聚( )| A、②③④ | B、①③⑤⑥ |
| C、①③④⑤ | D、②③④⑤⑥ |
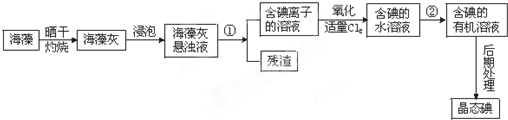
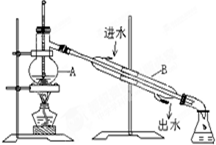 图中装置中仪器的名称:
图中装置中仪器的名称: