��Ŀ����
15�������£����и���������ָ����Һ��һ���ܴ���������ǣ�������| A�� | 0.1 mol•L-1NaNO3��Һ��H+��Fe2+��Cl-��SO42-��K+ | |
| B�� | $\frac{{K}_{W}}{c��{H}^{+}��}$=10-13mol•L-1����Һ��Na+��AlO2-��OH-��NO3- | |
| C�� | 0.1 mol•L-1NH3•H2O��Һ��K+��Na+��NO3-��C1- | |
| D�� | ���������ܲ�������H2����Һ��Na+��K+��Cl-��HCO3- |
���� A������������������������ܹ������������ӣ�
B������Һ�д��ڴ��������ӣ�ƫ��������ӡ������������������ӷ�Ӧ��
C����������֮�䲻��Ӧ�������백ˮ��Ӧ��
D�����������ܲ�������H2����Һ�д��ڴ��������ӻ����������ӣ�̼����������������ӡ����������ӷ�Ӧ��
��� �⣺A��NaNO3��H+��Fe2+֮�䷢��������ԭ��Ӧ������Һ�в��ܴ������棬��A����
B������ҺΪ������Һ����Һ�д��������ӣ�AlO2-��OH-��������֮�䷢����Ӧ������Һ�в��ܴ������棬��B����
C��K+��Na+��NO3-��C1-֮�䲻������Ӧ��������NH3•H2O��Ӧ������Һ���ܹ��������棬��C��ȷ��
D�����������ܲ�������H2����ҺΪ���Ի�ǿ������Һ����Һ�д��ڴ��������ӻ����������ӣ�HCO3-�������Ӻ����������ӷ�Ӧ������Һ�в��ܴ������棬��D����
��ѡC��
���� ���⿼�����ӹ���������жϣ�Ϊ�߿��ĸ�Ƶ�⣬�����е��Ѷȵ����⣬ע����ȷ���Ӳ��ܴ��������һ��������ܷ������ֽⷴӦ������֮�䣻�ܷ���������ԭ��Ӧ������֮�䣻�ܷ�����Ϸ�Ӧ������֮�䣨�� Fe3+�� SCN-���ȣ���Ӧ��ע����Ŀ���������������磺��Һ������ԣ��ݴ����ж���Һ���Ƿ��д����� H+��OH-����Һ�ľ��巴Ӧ�������硰������ԭ��Ӧ�������������۲������������ǡ����ܡ����棬���ǡ�һ��������ȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�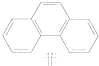
| A�� | �����һ�ȴ�����2�֣�����Ķ��ȴ�����4�� | |
| B�� | ����ʽΪC8H10�������ڷ����廯�����ͬ���칹��ֻ��3�� | |
| C�� | �ƵĽṹ��ʽ����ͼ���������ᷴӦ������һ����ȡ������5�� | |
| D�� | �ױ������ϵ�һ����ԭ�ӱ�һC3H7ȡ���������л�������6�� |
 �����ѣ�CH3OCH3����һ����Ҫ�����ȼ�ϣ�Ҳ�������������������ȣ��Գ��������ƻ����ã���ҵ����ˮú����CO��H2��Ϊԭ������������CH3OCH3���¹�����Ҫ����������Ӧ��
�����ѣ�CH3OCH3����һ����Ҫ�����ȼ�ϣ�Ҳ�������������������ȣ��Գ��������ƻ����ã���ҵ����ˮú����CO��H2��Ϊԭ������������CH3OCH3���¹�����Ҫ����������Ӧ��2H2��g��+CO��g��?CH3OH��g����H=-90.0kJ��mol-1 ��
2CH3OH��g��?CH3OCH��g��+H2O ��g����H=-24.5kJ��mol-1��
CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.1kJ��mol-1��
�ش��������⣺
��1���¹��յ��ܷ�Ӧ3H2+3CO?CH3OCH3+CO2���Ȼ�ѧ����ʽΪ3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g����H=-245.6kJ/mol��
��2����֪һЩ���ۼ��ļ������£�
| ��ѧ�� | H-H | C-H | C-O | O-H |
| ���ܣ�kJ��mol-1 | 436 | 414 | 326 | 464 |
��3����250������ܱ������У�������ʵ����˵����Ӧ���Ѵ�ƽ����ǣ���ѡ����ĸ��BC��
A�������������ܶȱ��ֲ���
B��CO��CO2�����ʵ���֮�ȱ��ֲ���
C��H2O��CO2����������֮��Ϊ1��1
D���÷�Ӧ��ƽ�ⳣ�����ֲ���
��4��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c��CO��=0.2mol/L��������¶��µ�ƽ�ⳣ��K=2.042��
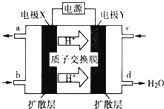
��5����ɫ��Դ��������-����ȼ�ϵ�ء��Ĺ���ԭ����ͼ��ʾ��
������Ӧ��C��ͨ�룬�缫YΪ�����������ĵ缫��ӦʽΪO2+4e-+4H+�T2H2O��
�ڶ����ѣ�CH3��2OӦ��b�����룬�缫X�Ϸ����ĵ缫��ӦʽΪ��CH3��2O-12e-+3H2O=2CO2+12H+��
�۵���ڷŵ�����У��缫X��Χ��Һ��pH��С ���������С�����䡱����
| A�� | ��������ʯ��ǿ�ȶ����ֽ� | |
| B�� | ��������ʯ������ǿ����� | |
| C�� | ��������ʯ���Ⱥ������Ӽ��ֺ��й��ۼ� | |
| D�� | ������������������ʯ�е�K+�ڻ���������ʱ���ֳ�������ɫ |
| ʵ��Ŀ�� | ʵ�鷽�� | ��ѡ�������� | |
| A | ��ȥ���������������Ҵ� | ��������м�ˮ�����ˮϴ��Һ | ��Һ©�����ձ� |
| B | ֤��HClO�ʹ��������ǿ�� | ͬ������pH��ֽ�ⶨŨ��Ϊ0.1mol•L-1NaClO��Һ��0.1mol•L-1CH3COONa��Һ��pH | ������������Ƭ |
| C | ��FeCl3��Һ�õ�FeCl3•6H2O���� | ��FeCl3��Һ�в��ϵμ����ᣬ���ȣ����о��� ���� | �ƾ��ơ����������� |
| D | ����1L 0.1mol•L-1��CuSO4��Һ | ��16gCuSO4•5H2O����ˮ���1000mL��Һ | �ձ�����Ͳ����������1000mL����ƿ |
| A�� | A | B�� | B | C�� | C | D�� | D |
| ѡ�� | ʵ�� | ���� | ���� |
| A | ������Xͨ��Ʒ����Һ�����Ը��������Һ | ����Һ����ɫ | X��������ϩ |
| B | �������Һ�м���ϡH2SO4��ˮԡ���ȼ����ӣ���ȴ���ټ�������Cu��OH��2����Һ������ | ��ש��ɫ�������� | ��������û��ˮ������������ |
| C | ����Cl-��SO42-��Һ�У�������������ữ��Ba��NO3��2��Һ�����ˣ�����Һ���ٵμ�AgNO3��Һ | �а�ɫ�������� | ֤����Һ����Cl- |
| D | ��ʢ��5mL0.005mol•L-1 FeCl3��Һ���Թ��м���5mL0.01mol•L 1KSCN��Һ���ټ���4��0.1mol•L -1KSCN��Һ | ��Һ��ɫ���� | Fe3++3SCN-?Fe��SCN��3���淴Ӧ |
| A�� | A | B�� | B | C�� | C | D�� | D |

 ��
��