题目内容
6.下列物质溶于水后由于水解而显酸性的是( )| A. | NaHSO4 | B. | NaHCO3 | C. | FeCl3 | D. | CH3COOH |
分析 因发生水解而显酸性的物质为强酸弱碱盐,弱碱阳离子结合水电离出的氢氧根离子促进了水的电离,溶液氢氧根离子浓度大于氢离子浓度,溶液呈酸性,据此进行解答.
解答 解:A.NaHSO4为强酸的酸式盐,在溶液中完全电离:NaHSO4=Na++H++SO42-,溶液呈酸性,但不是由于水解的原因,故A不选;
B.NaHCO3为强碱弱酸盐,水解呈碱性,故B不选;
C.FeCl3为强酸弱碱盐,铁离子发生水解呈酸性,故C选;
D.醋酸为一元强酸,电离子出氢离子,溶液呈酸性,不是水解的原因,故D不选;
故选C.
点评 本题考查盐类水解的应用,侧重于学生的分析能力的考查,题目难度不大,明确盐类水解的规律以及水解原理为解答关键,注意相关基础知识的积累.

练习册系列答案
相关题目
16.分类方法在化学教材必修I中出现,下列分类标准合理的是( )
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②根据化学反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③CO、NO、N2O、NO2、N2O4、ClO2等形不成同价态的盐,故他们不是酸性氧化物
④根据反应中的热效应将化学反应分为放热反应和吸热反应.
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②根据化学反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③CO、NO、N2O、NO2、N2O4、ClO2等形不成同价态的盐,故他们不是酸性氧化物
④根据反应中的热效应将化学反应分为放热反应和吸热反应.
| A. | ①②③ | B. | ①③④ | C. | ①②④ | D. | ②③④ |
1.在一密闭容器中进行下列反应:2SO2(g)+O2(g)?2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达到平衡时,可能存在的数据是( )
| A. | SO2为0.4mol/L,O2为0.2mol/L | B. | SO2为0.15mol/L | ||
| C. | SO2,SO3均为0.25mol/L | D. | SO3为0.4mol/L |
11.下列分子式只表示一种物质的是( )
| A. | C6H12O6 | B. | (C6H10O5)n | C. | C12H22O11 | D. | CF2Cl2 |
18.下列4组已知原子序数的元素,彼此间能形成共价键的是( )
| A. | 8和11 | B. | 19和17 | C. | 6和16 | D. | 12和9 |
16.将盛有N2和NO2的混合气体的试管倒立于水中经过足够时间后,气体体积减少为原来的$\frac{3}{4}$,则原混合气体中N2和NO2的体积比是( )
| A. | 1:1 | B. | 1:2 | C. | 5:3 | D. | 3:2 |
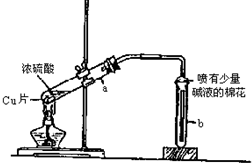 如图为浓硫酸与铜反应的实验装置图.
如图为浓硫酸与铜反应的实验装置图.