题目内容
4.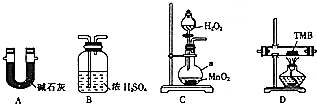 由碳、氢、氮三种元素组成的TMB是一种新型指纹检测的色原试剂,其相对分子质量为240.某研究性学习小组的同学欲利用下列装置测定TMB的分子式.实验原理:在足量氧气流中将4.80gTMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2.请从图中选择适当的装置(部分装置可以重复)进行实验.
由碳、氢、氮三种元素组成的TMB是一种新型指纹检测的色原试剂,其相对分子质量为240.某研究性学习小组的同学欲利用下列装置测定TMB的分子式.实验原理:在足量氧气流中将4.80gTMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2.请从图中选择适当的装置(部分装置可以重复)进行实验.(1)仪器a的名称为圆底烧瓶.
(2)实验装置依次连接的顺序为CBDBAA.
(3)写出装置C中反应的化学方程式:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
(4)该实验不需要(填“需要”或“不需要”)尾气处理,理由是碳元素必须燃烧完全才能保证实验结果的准确性,没有有毒气体放出.
(5)实验后称得装置A的质量增加14.08g,装置B的质量增加3.60g并收集到0.56g氮气(假设每次吸收均是完全的),则TMB的分子式为C16H20N2.
(6)设计实验验证CO2具有氧化性:将打磨过的镁条点燃后深入充满二氧化碳的集气瓶中,镁条继续燃烧,集气瓶中有黑色固体生成为碳单质,说明二氧化碳具有氧化性.
分析 C中过氧化氢在二氧化锰催化作用下生成氧气,用浓硫酸干燥氧气,氧气将TMB氧化为二氧化碳、水和氮气,用碱石灰吸收二氧化碳,.根据A装置增加14.08g可以求出样品中C元素的物质的量,B装置增加3.60g可以求出样品中H元素的物质的量,再根据收集到0.56g氮气可以求出样品中N元素的物质的量,则TMB分子中碳、氢、氮的原子个数比就可以求出,根据相对分子质量之比算出相对分子质量,结合原子个数比计算出分子式,以此解答该题,
(1)仪器a为圆底烧瓶
(2)依据上述分析可知装置连接为制备氧气、干燥氧气、将TMB氧化、浓硫酸吸收生成的水蒸气、碱石灰吸收生成的二氧化碳气体、最后连接碱石灰防止空气中的二氧化碳和水蒸气进入装置A干扰测定结果;
(3)过氧化氢在二氧化锰作用下分解生成水和氧气;
(4)因二氧化碳完全吸收,且生成氮气,没有必要进行尾气处理;
(5)实验后称得装置从用的先后顺序排列质量分别增加3.60g、14.08g,收集到0.56g氮气,则m(H2O)=3.60g,m(CO2)=14.08g,则
n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,n(H)=0.4mol,
n(CO2)=$\frac{14.08g}{44g/mol}$=0.32mol,n(C)=0.32mol,
所以n(N)=$\frac{0.56g}{14g/mol}$=0.04mol,
则:n(C):n(H):n(N)=0.32mol:0.4mol:0.04mol=8:10:1,
依据相对分子质量计算分子式;
(6)设计实验使二氧化碳发生反应后碳元素化合价降低,做氧化剂,如镁条在二氧化碳中燃烧生成碳;
解答 解:C中过氧化氢在二氧化锰催化作用下生成氧气,用浓硫酸干燥氧气,氧气将TMB氧化为二氧化碳、水和氮气,用碱石灰吸收二氧化碳,.根据A装置增加14.08g可以求出样品中C元素的物质的量,B装置增加3.60g可以求出样品中H元素的物质的量,再根据收集到0.56g氮气可以求出样品中N元素的物质的量,则TMB分子中碳、氢、氮的原子个数比就可以求出,根据相对分子质量之比算出相对分子质量,结合原子个数比计算出分子式,以此解答该题,
(1)依据图形和作用可知,仪器a为圆底烧瓶,
故答案为:圆底烧瓶;
(2)依据上述分析可知装置连接为制备氧气、干燥氧气、将TMB氧化、浓硫酸吸收生成的水蒸气、碱石灰吸收生成的二氧化碳气体、最后连接碱石灰防止空气中的二氧化碳和水蒸气进入装置A干扰测定结果,装置连接顺序为:CBDBAA,
故答案为:CBDBAA;
(3)过氧化氢在二氧化锰作用下分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑,
故答案为:2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;
(4)因二氧化碳完全吸收,且生成氮气是空气的成分,没有必要进行尾气处理,
故答案为:不需要;因为碳元素必须燃烧完全才能保证实验结果的准确性,没有有毒气体排放;
(5)实验后称得装置从用的先后顺序排列质量分别增加3.60g、14.08g,收集到0.56g氮气,则m(H2O)=3.60g,m(CO2)=14.08g,则
n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,n(H)=0.4mol,
n(CO2)=$\frac{14.08g}{44g/mol}$=0.32mol,n(C)=0.32mol,
所以n(N)=$\frac{0.56g}{14g/mol}$=0.04mol,
则:n(C):n(H):n(N)=0.32mol:0.4mol:0.04mol=8:10:1,
TMB的相对分子质量为:2×120=240,设分子式为:C8nH10nNn,则有:12×8n+10n+14n=240,解得n=2,所以分子式为C16H20N2,
故答案为:C16H20N2;
(6)设计实验使二氧化碳发生反应后碳元素化合价降低,做氧化剂,将打磨过的镁条点燃后深入充满二氧化碳的集气瓶中,镁条继续燃烧,集气瓶中有黑色固体生成为碳单质,说明二氧化碳具有氧化性,
故答案为:将打磨过的镁条点燃后深入充满二氧化碳的集气瓶中,镁条继续燃烧,集气瓶中有黑色固体生成为碳单质,说明二氧化碳具有氧化性;
点评 本题考查了物质组成和性质的探究,生成产物的实验验证设计,化学式的计算应用等知识点,主要是测定个成分的实验装置作用的理解应用,题目难度中等.

| t/min | t0 | t1 | t2 | t3 | t4 | t5 |
| Φ(NO2) | $\frac{1}{3}$ | 0.30 | $\frac{4}{15}$ | $\frac{1}{6}$ | $\frac{1}{15}$ | $\frac{1}{15}$ |
| Φ(SO2) | $\frac{2}{3}$ | $\frac{19}{30}$ | 0.60 | 0.50 | 0.40 | 0.40 |
a.体系压强保持不变 b.混合气体颜色保持不变
c.反应的焓变保持不变 d.每消耗1mol SO3同时生成1 mol SO2
②根据上述实验结果,该温度下反应的平衡常数K的计算结果为$\frac{8}{3}$(不用小数表示).
③上述反应中,正反应速率为v正=k正Φ(NO2)Φ(SO2),逆反应速率v逆=k逆Φ(SO3)Φ(NO),其中k正、k逆为速率常数,则k正=K•k逆(以K和k逆表示)
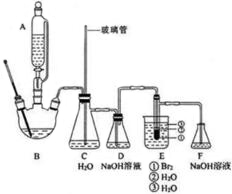 1,2-二溴乙烷是常用的有机合成中间体,某小组用如下装置合成1,2-二溴乙烷.
1,2-二溴乙烷是常用的有机合成中间体,某小组用如下装置合成1,2-二溴乙烷.装置B中发生的反应为C2H5OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2↑+H2O
产物和部分反应物的相关数据如下:
| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 1,2-二溴乙烷 | 131.4 | 2.18 | 微溶 |
| 溴 | 58.8 | 3.12 | 微溶 |
| 乙醇 | 78.5 | 0.79 | 溶 |
在冰水浴冷却下将20.0mL浓硫酸与10.0mL95%乙醇混合均匀地到反应液,取出10.0mL加入三颈烧瓶B中,剩余部分装入滴液漏斗A中.E的试管中加入8.0g液溴,再加入2-3mL水,使管外用水冷却.断开D、E之间的导管,加热B,待装置内空气被排除后,连接D和E,继续加热并保持温度在170-180℃,打开滴液漏斗活塞,缓慢滴加反应液,直至反应完毕.
分离提纯:
将粗产物分别用10%的氢氧化钠溶液和水洗涤,分离后加入无水氯化钙干燥,待溶液澄清后进行蒸馏,得到纯净的1,2-二溴乙烷6.3g.
回答下列问题:
(1)混合浓硫酸与乙醇时,加入试剂的正确顺序是先加乙醇,再加浓硫酸;使用冰水浴降温的目的是防止乙醇挥发.
(2)为防止暴沸,装置B中还应加入碎瓷片;C的作用是平衡气压;E中试管里加水的目的是防止溴、产物1,2-二溴乙烷挥发.
(3)判断生成1,2-二溴乙烷反应结束的方法是E中试管里的液体变为无色;反应结束时正确的操作是断开DE之间的导管,再停止加热.
(4)洗涤和分离粗产物时使用的玻璃仪器是分液漏斗、烧杯.
(5)本实验中,1,2-二溴乙烷的产率为67%.
(6)下列操作中,将导致产物产率降低的是abc(填正确答案的标号).
a.乙烯通入溴时迅速鼓泡 b.实验室没有装置D
c.去掉装置E烧杯中的水 d.装置F中NaOH溶液用水代替.
| 实验操作 | 现象和结论 | |
| A | 在平衡3KSCN+FeCl3?Fe(SCN)3+3KCl的溶液中加入少量KCl溶液 | 溶液红色变浅,平衡逆向移动 |
| B | 向AgI沉淀中滴入KCl溶液 | 有白色沉生成,Ksp(AgCl)<Ksp(AgI) |
| C | 把Cl2通入品红溶液中 | 溶液褪色,Cl2具有漂白性 |
| D | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液 | 溶液变为黄色,氧化性:H2O2>Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氢键;分子间作用力;非极性键 | B. | 氢键;极性键;非极性键 | ||
| C. | 氢键;极性键;分子间作用力 | D. | 分子间作用力;氢键;非极性键 |
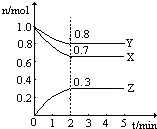 某温度时,在一个2L恒容的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L恒容的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: