题目内容
下列有关平衡常数的说法中,正确的是( )
| A、改变条件,反应物的转化率增大,平衡常数也一定增大 | ||||||
| B、反应2NO2(g)═N2O4(g)△H<0,升高温度该反应平衡常数增大 | ||||||
| C、对于给定可逆反应,温度一定时,其正、逆反应的平衡常数相等 | ||||||
D、CO2+H2
|
考点:化学平衡常数的含义
专题:
分析:平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比,K越大,反应物的转化率越大,而且平衡常数是温度的函数,据此分析解答.
解答:
解:A、改变条件,反应物的转化率增大,如果温度不变,平衡常数不变,故A错误;
B、正反应是放热反应,温度升高K变小,故B错误;
C、于给定可逆反应,温度一定时,如果平衡常数等于1,其正、逆反应的平衡常数才相等,故C错误;
D、CO2+H2
CO+H2O的平衡常数表达式为 K=
,故D正确;
故选D.
B、正反应是放热反应,温度升高K变小,故B错误;
C、于给定可逆反应,温度一定时,如果平衡常数等于1,其正、逆反应的平衡常数才相等,故C错误;
D、CO2+H2
| ||
| 高温 |
| [CO][H2O] |
| [CO2][H2] |
故选D.
点评:明确化学平衡K的含义是解本题关键,知道K值大小的影响因素,知道所有的平衡常数只与温度有关,与物质的浓度无关,化学平衡常数表达式中不含固体和纯液体,为易错点.

练习册系列答案
相关题目
钙是人体必需的常量元素,成年人每天需要800mg的钙,下列补钙的方式不正确的是( )
| A、经常晒太阳 |
| B、经常饮用钙离子含量高的硬水 |
| C、经常饮用牛奶、豆奶 |
| D、补充维生素D |
下列离子既能电离又能水解,且能与强碱溶液反应的是( )
| A、CH3COO- |
| B、HSO4- |
| C、HSO3- |
| D、CO32- |
节能减排对发展经济、保护环境具有重要意义.下列措施不能减少二氧化碳排放的是( )
| A、利用太阳能制氢 |
| B、关停小火电企业 |
| C、举行“地球一小时”熄灯活动 |
| D、推广使用煤液化技术 |
反应N2+O2=2NO,在密闭容器中进行,一定能加快该反应速率的是( )
| A、使压强增大 |
| B、体积不变充入N2使压强增大 |
| C、体积不变充入He使压强增大 |
| D、压强不变充入N2使体积增大 |
下列物质的用途错误的是( )
| A、氯气用于自来水杀菌消毒 |
| B、晶体硅用于制造光导纤维 |
| C、氨用于制备硝酸 |
| D、氧化铁用于制造红色涂料 |
下列各表述与示意图一致的是( )
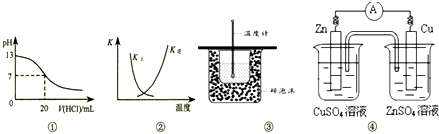

| A、图①表示25℃时,用0.1 mol?L-1盐酸滴定20 mL 0.1 mol?L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
| B、图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 |
| C、图③装置用于测定中和热 |
| D、图④装置可以构成锌、铜、硫酸铜溶液原电池 |
碳原子的摩尔质量是( )
| A、12 | B、12g/mol |
| C、12mol | D、12g |