题目内容
7.对下列实验操作对应的实验现象和结论的描述正确的是( )| 选项 | 实验操作 | 实验现象与结论 |
| A | 将40gNaOH固体溶于1.0L蒸馏水中配成溶液 | 所配NaOH溶液溶质物质的量浓度为1.0mol/L |
| B | 用洁净的铂丝蘸取某待测液在酒精灯外焰上灼烧 | 火焰呈黄色,证明待测试液中一定含有钠元素 |
| C | 向品红溶液中通入某气体 | 品红溶液褪色,则该气体一定是SO2 |
| D | 向某取色溶液中滴加稀硝酸酸化后,再滴加BaCl2溶液 | 产生白色沉淀,证明该溶液中一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溶于1.0L蒸馏水,为溶剂的体积;
B.焰色反应为元素的性质;
C.氯气、二氧化硫均使品红溶液褪色;
D.白色沉淀可能为AgCl或硫酸钡.
解答 解:A.溶于1.0L蒸馏水,为溶剂的体积,溶液体积未知,不能计算浓度,故A错误;
B.焰色反应为元素的性质,由焰色反应为黄色,可知试液中一定含有钠元素,故B正确;
C.氯气、二氧化硫均使品红溶液褪色,则品红溶液褪色,则该气体可能是SO2,故C错误;
D.白色沉淀可能为AgCl或硫酸钡,则该溶液中可能含有SO42-,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握溶液的配制、焰色反应、物质的性质、离子检验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.25℃时,三种浓度均为0.1mol•L-1的溶液pH如下表,下列说法正确的是( )
| 序号 | ① | ② | ③ |
| 溶液 | NaClO | NaHCO3 | Na2CO3 |
| pH | 10.3 | 8.3 | 11.6 |
| A. | 酸性:HClO>H2CO3 | |
| B. | 由水电离产生的c(OH-):①>② | |
| C. | 溶液①中的c(ClO-)大于溶液②中的c(HCO3-) | |
| D. | 溶液③中:c(HCO3-)+c(CO32-)=0.1 mol•L-1 |
15.欲除去碳酸钠固体中混有的少量碳酸氢钠,最好的方法是( )
| A. | 将固体加热至不再有气体产生 | |
| B. | 将固体配成溶液,再加入过量的澄清石灰水 | |
| C. | 将固体配成溶液,再加入过量的NaOH溶液 | |
| D. | 将固体配成溶液,再通入足量的CO2气体 |
2.下列措施肯定能加快化学反应速率的是( )
| A. | 增大压强 | B. | 升高温度 | ||
| C. | 使用催化剂 | D. | 增加反应物的用量 |
12.在下列溶液中,各组离子可能大量共存的是( )
| A. | 由水电离的c(H+)=1×10-4 mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| B. | 在pH=1的无色溶液中:Fe2+、Mg2+、NO3-、SO42- | |
| C. | c(K2C2O4)=1mol/L溶液中:Na+、Cl-、MnO4-、K+ | |
| D. | 能与铝反应产生H2的溶液中:Mg2+、SO42-、K+、Cl- |
19.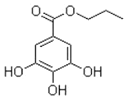 没食子酸丙酯简称PG,结构简式如图,可用于食品油脂、油炸食品、干鱼制品、饼干、方便面等,是联合国粮农组织和世界卫生组织批准使用的优良油脂抗氧化剂之一.则下列说法正确的是( )
没食子酸丙酯简称PG,结构简式如图,可用于食品油脂、油炸食品、干鱼制品、饼干、方便面等,是联合国粮农组织和世界卫生组织批准使用的优良油脂抗氧化剂之一.则下列说法正确的是( )
 没食子酸丙酯简称PG,结构简式如图,可用于食品油脂、油炸食品、干鱼制品、饼干、方便面等,是联合国粮农组织和世界卫生组织批准使用的优良油脂抗氧化剂之一.则下列说法正确的是( )
没食子酸丙酯简称PG,结构简式如图,可用于食品油脂、油炸食品、干鱼制品、饼干、方便面等,是联合国粮农组织和世界卫生组织批准使用的优良油脂抗氧化剂之一.则下列说法正确的是( )| A. | 没食子酸丙酯的分子式是 C10Hl3O5 | |
| B. | 1mol没食子酸丙酯能与4mol H2加成 | |
| C. | 1mol没食子酸丙酯能与4mol NaOH反应 | |
| D. | 1mol没食子酸丙酯最多能与3mol浓溴水发生取代反应 |
15.Cl2和SO2都具有漂白作用,能使品红溶液褪色.若将等物质的量的Cl2、SO2混合后,再通入品红溶液与BaCl2的混合溶液,能观察到的现象是( )
| A. | 溶液很快褪色,出现沉淀 | B. | 溶液不褪色,不出现沉淀 | ||
| C. | 溶液不褪色,出现沉淀 | D. | 溶液很快褪色,不出现沉淀 |
16.下列说法正确的是( )
| A. | 镀锡铁表面划损时,仍然能阻止铁被腐蚀 | |
| B. | 锌和稀硫酸反应时,加人铜粉可使反应加快 | |
| C. | 将镁、铝用导线连接后放人NaOH溶液中,镁作负极 | |
| D. | 原电池负极上发生的反应是还原反应 |