题目内容
15.欲除去碳酸钠固体中混有的少量碳酸氢钠,最好的方法是( )| A. | 将固体加热至不再有气体产生 | |
| B. | 将固体配成溶液,再加入过量的澄清石灰水 | |
| C. | 将固体配成溶液,再加入过量的NaOH溶液 | |
| D. | 将固体配成溶液,再通入足量的CO2气体 |
分析 碳酸氢钠加热分解生成碳酸钠,则加热可除去碳酸钠固体中混有的少量碳酸氢钠,以此来解答.
解答 解:A.将固体加热至不再有气体产生,碳酸氢钠完全分解生成碳酸钠、水、二氧化碳,可除杂,故A选;
B.二者均与石灰水反应生成白色沉淀,不能除杂,故B不选;
C.加入过量的NaOH溶液,引入新杂质NaOH,故C不选;
D.配成溶液,再通入足量的CO2气体,将原物质除去,故D不选;
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.已知弱酸等弱电解质电离时吸热.在测定中和热的实验中,下列说法正确的是( )
| A. | 为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 | |
| B. | 使用环形玻璃搅拌棒是为了加大反应速率,减小实验误差 | |
| C. | 用0.5mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 | |
| D. | 在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计 |
6.下列图示装置的实验中,操作正确且能达到实验目的是( )
| A. |  如图:用食盐水制食盐晶体 | B. |  如图:分离碘酒中的碘和酒精 | ||
| C. |  如图:稀释浓硫酸 | D. | 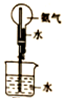 如图:验证氨水的碱性 |
3.下列措施不能加快Zn与1mol/LH2SO4反应产生H2的速率的是( )
| A. | 升高温度 | B. | 用Zn粉代替Zn粒 | ||
| C. | 滴加少量的CuSO4溶液 | D. | 改用0.1mol/LH2SO4与Zn反应 |
10.下列对于氨气“喷泉实验”(如图所示)的现象或结论的描述正确的是( )


| A. | 烧杯中的水面会缓缓上升 | |
| B. | 烧瓶内形成蓝色喷泉 | |
| C. | 实验证明氨气极易溶于水 | |
| D. | 实验证明氨气的密度大于空气的密度 |
20.下列反应的离子方程式中,正确的是( )
| A. | 铁和稀盐酸反应:2 Fe+6H+═2Fe3++3 H2↑ | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 碳酸钙溶于稀盐酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 碳酸氢钠溶液中滴入NaOH溶液:HCO3-+OH-═H2O+CO2↑ |
7.对下列实验操作对应的实验现象和结论的描述正确的是( )
| 选项 | 实验操作 | 实验现象与结论 |
| A | 将40gNaOH固体溶于1.0L蒸馏水中配成溶液 | 所配NaOH溶液溶质物质的量浓度为1.0mol/L |
| B | 用洁净的铂丝蘸取某待测液在酒精灯外焰上灼烧 | 火焰呈黄色,证明待测试液中一定含有钠元素 |
| C | 向品红溶液中通入某气体 | 品红溶液褪色,则该气体一定是SO2 |
| D | 向某取色溶液中滴加稀硝酸酸化后,再滴加BaCl2溶液 | 产生白色沉淀,证明该溶液中一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
4.对处于平衡状态的反应2A(g)+B(g)?2C(g)△H<0,下列叙述正确的是 ( )
| A. | 升高温度,v正减小,v逆增大 | |
| B. | 增大A浓度的瞬间,v正增大,v逆不变 | |
| C. | 增大压强,v正增大,v逆减小 | |
| D. | 加入正催化剂,v正增大,v逆减小 |