题目内容
18.25℃时,三种浓度均为0.1mol•L-1的溶液pH如下表,下列说法正确的是( )| 序号 | ① | ② | ③ |
| 溶液 | NaClO | NaHCO3 | Na2CO3 |
| pH | 10.3 | 8.3 | 11.6 |
| A. | 酸性:HClO>H2CO3 | |
| B. | 由水电离产生的c(OH-):①>② | |
| C. | 溶液①中的c(ClO-)大于溶液②中的c(HCO3-) | |
| D. | 溶液③中:c(HCO3-)+c(CO32-)=0.1 mol•L-1 |
分析 A.盐溶液PH越大,碱性越强,说明对应酸的酸性越弱;
B.次氯酸根离子水解程度大于碳酸氢根离子,对水电离促进程度大;
C.次氯酸根离子水解程度大于碳酸氢根离子浓度,减少的多;
D.碳酸钠溶液中存在物料守恒.
解答 解:A.NaClO溶液PH=10.3、NaHCO3溶液PH=8.3,说明次氯酸根离子水解程度大于碳酸氢根离子,则对应酸的酸性HClO<H2CO3,故A错误;
B.次氯酸根离子水解程度大于碳酸氢根离子,对水电离促进程度大,由水电离产生的c(OH-):①NaClO>②NaHCO3,故B正确;
C.次氯酸根离子水解程度大于碳酸氢根离子浓度,减少的多,溶液①中的c(ClO-)小于溶液②中的c(HCO3-),故C错误;
D.碳酸钠溶液中存在物料守恒,c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol•L-1,故D错误;
故选B.
点评 本题考查了盐类水解、电解质溶液中电荷守恒和物料守恒,依据盐类水解判断对应酸的酸性强弱,掌握基础是解题关键,题目难度中等.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
13.下列各组离子在溶液中能大量共存的是( )
| A. | Cu2+、Mg2+、SO42-、NO3- | B. | H+、Mg2+、SO42-、HCO3- | ||
| C. | Ag+、Na+、NO3-、Cl- | D. | NH4+、Ba2+、NO3-、OH- |
9.下列各组离子在强酸性溶液中能大量共存的是( )
| A. | K+、Na+、HCO3-、SO42- | B. | Na+、Fe3+、I-、CI- | ||
| C. | Na+、NH4+、NO3-、CI- | D. | Na+、Ba2+、SO42-、NO3- |
6.下列图示装置的实验中,操作正确且能达到实验目的是( )
| A. |  如图:用食盐水制食盐晶体 | B. |  如图:分离碘酒中的碘和酒精 | ||
| C. |  如图:稀释浓硫酸 | D. | 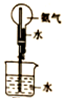 如图:验证氨水的碱性 |
13.常温下,加水稀释10mL 0.1mol•L-1CH3COOH溶液的过程中,下列数值中始终保持增大趋势的是( )
| A. | c(H+) | B. | Ka | ||
| C. | c(OH-) | D. | $\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ |
3.下列措施不能加快Zn与1mol/LH2SO4反应产生H2的速率的是( )
| A. | 升高温度 | B. | 用Zn粉代替Zn粒 | ||
| C. | 滴加少量的CuSO4溶液 | D. | 改用0.1mol/LH2SO4与Zn反应 |
10.下列对于氨气“喷泉实验”(如图所示)的现象或结论的描述正确的是( )


| A. | 烧杯中的水面会缓缓上升 | |
| B. | 烧瓶内形成蓝色喷泉 | |
| C. | 实验证明氨气极易溶于水 | |
| D. | 实验证明氨气的密度大于空气的密度 |
7.对下列实验操作对应的实验现象和结论的描述正确的是( )
| 选项 | 实验操作 | 实验现象与结论 |
| A | 将40gNaOH固体溶于1.0L蒸馏水中配成溶液 | 所配NaOH溶液溶质物质的量浓度为1.0mol/L |
| B | 用洁净的铂丝蘸取某待测液在酒精灯外焰上灼烧 | 火焰呈黄色,证明待测试液中一定含有钠元素 |
| C | 向品红溶液中通入某气体 | 品红溶液褪色,则该气体一定是SO2 |
| D | 向某取色溶液中滴加稀硝酸酸化后,再滴加BaCl2溶液 | 产生白色沉淀,证明该溶液中一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
7.下列反应中,调节反应物用量或浓度会改变反应产物的是( )
| A. | H2S在氧气中燃烧 | B. | H2SO4中加入锌粉 | ||
| C. | SO2通入溴水 | D. | 铁在硫蒸气中加热 |