题目内容
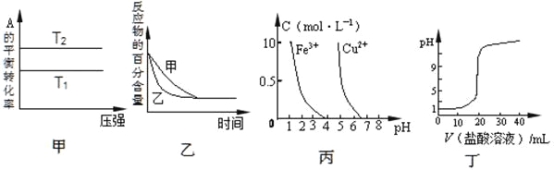
【题目】如图所示与对应叙述相符的是![]()

A.图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则![]()
B.图乙表示![]() 的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸
的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸![]() 乙酸
乙酸
C.图丙是用![]() 0
0![]() 溶液滴定
溶液滴定![]() mL盐酸的滴定曲线
mL盐酸的滴定曲线
D.图丁表示反应![]() 平衡时
平衡时![]() 体积分数随起始
体积分数随起始![]() 变化的曲线,则转化率:
变化的曲线,则转化率:![]()
【答案】A
【解析】
A.![]() 的浓度相同时,由图象可知,平衡时
的浓度相同时,由图象可知,平衡时![]() ,则
,则![]() ,根据
,根据![]() ,
,![]() ,则
,则![]() ,故A正确;
,故A正确;
B.由图可知,稀释相同的倍数,甲酸的pH变化大,则甲酸的酸性比乙酸强,即酸性:甲酸![]() 乙酸,故B错误;
乙酸,故B错误;
C.用![]() 的NaOH溶液滴定
的NaOH溶液滴定![]() 的盐酸溶液,由图象可知,当消耗NaOH体积为
的盐酸溶液,由图象可知,当消耗NaOH体积为![]() 时,溶液为中性,此时酸和碱恰好完全反应,但并不知道盐酸的浓度,图像并不一定为真,故C错误;
时,溶液为中性,此时酸和碱恰好完全反应,但并不知道盐酸的浓度,图像并不一定为真,故C错误;
D.随着 值增大,可认为是增加了
值增大,可认为是增加了![]() 的量,从而提高了
的量,从而提高了![]() 的转化率,所以转化率
的转化率,所以转化率![]() ,故D错误。
,故D错误。
故选:A。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】几种主族元素(过渡元素略去)在周期表中的位置如下:
A | |||||||
M | B | D | |||||
E | G | R | J | ||||
T | |||||||
(1)E、G、T的原子半径由大到小的顺序是_____(填元素符号)。
(2)硒元素(34Se)与D同主族,其非金属性比D______(填“强”或“弱”)。
(3)E、G元素最高价氧化物对应水化物之间能反应,离子方程式为:_______。
(4)E、D两元素能形成原子个数比1:1 型化合物的电子式为________。
(5)A与M形成的分子可能是________(填字母序号)。

【题目】25℃时,浓度均为0.1 mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A.酸性强弱:H2CO3>HF
B.①和②中溶质均未水解
C.离子的总浓度:①>③
D.④中:c(HCO3-) + 2c(CO32-) + c(H2CO3)![]() 0.1 mol/L
0.1 mol/L