题目内容
(16分)某科研小组以难溶性钾长石(K2O·Al2O3·6SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下: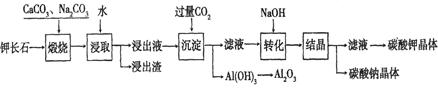
(1)煅烧过程中有如下反应发生:
①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式: 。
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式: 。
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2-+ 2H2O Al(OH)3+ OH-。“浸取”时应保持溶液呈________性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_____ ____。
Al(OH)3+ OH-。“浸取”时应保持溶液呈________性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_____ ____。
(3)“转化”时加入NaOH的主要作用是(用离子方程式表示)_____ ____。
(4)上述工艺中可以循环利用的主要物质是____ ____、_____ ___和水。
(1)①CaCO3+SiO2 CaSiO3+CO2↑(2分); ②Na2CO3+Al2O3
CaSiO3+CO2↑(2分); ②Na2CO3+Al2O3 2NaAlO2+CO2↑(2分)
2NaAlO2+CO2↑(2分)
(2)碱(2分);提高浸取速率(或增大原料浸出率,3分)
(3)HCO3-+OH-=H2O+ CO32-(3分);(4)Na2CO3、CO2(4分,各2分)。
解析试题分析:(1)①SiO2转化为CaSiO3的化学方程式是CaCO3+SiO2 CaSiO3+CO2↑;②Al2O3转化为NaAlO2的化学方程式是:Na2CO3+Al2O3
CaSiO3+CO2↑;②Al2O3转化为NaAlO2的化学方程式是:Na2CO3+Al2O3 2NaAlO2+CO2↑;(2)由于NaAlO2和KAlO2易发生如下水解反应:AlO2-+ 2H2O
2NaAlO2+CO2↑;(2)由于NaAlO2和KAlO2易发生如下水解反应:AlO2-+ 2H2O Al(OH)3+ OH-。所以 “浸取”时应保持溶液呈碱性以抑制盐的水解,“浸取”时不断搅拌的目的是提高浸取速率(或增大原料浸出率);(3)“转化”时加入NaOH的主要作用是HCO3-+OH-=H2O+ CO32-;(4)上述工艺中可以循环利用的主要物质是Na2CO3、CO2、和水。
Al(OH)3+ OH-。所以 “浸取”时应保持溶液呈碱性以抑制盐的水解,“浸取”时不断搅拌的目的是提高浸取速率(或增大原料浸出率);(3)“转化”时加入NaOH的主要作用是HCO3-+OH-=H2O+ CO32-;(4)上述工艺中可以循环利用的主要物质是Na2CO3、CO2、和水。
考点:考查物质的转化过程中反应原理、反应条件的选择、盐的水解、化学方程式、离子方程式的书写、物质的循环利用的知识。

保存少量金属钠的方法是
| A.放在冰水中 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
把4.6g钠投放到195.4g水中,所得溶液的质量分数为
| A.2.3% | B.大于2.3% | C.4% | D.大于4% |
有铁的氧化物样品,用140ml0.5mol/L的盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下氯气56ml,使其中的Fe2+全部转化为Fe3+,该样品可能的化学式是( )
| A.Fe2O3 | B.Fe3O4 | C.Fe5O7 | D.Fe4O5 |
(15分)用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/LFeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值:)
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| I | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| II | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| III | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)I中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的方程式_____。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_____性。
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
②IV中检测Cl2的实验方法:____________________。
③与II对比,得出的结论(写出两点):___________________。
切开的金属Na暴露在空气中,其变化过程如下:
(1)反应Ⅰ的反应过程与能量变化的关系如下:
① 反应Ⅰ 是 反应(填“放热”或“吸热”),判断依据是 。
② 1 mol Na(s)全部氧化成Na2O(s)的热化学方程式是 。
(2)反应Ⅱ是Na2O与水的反应,其产物的电子式是 。
(3)白色粉末为Na2CO3。将其溶于水配制为0.1 mol/L Na2CO3溶液,下列说法正确的是 (填字母)。
| A.升高温度,溶液的pH降低 |
| B.c(OH-)-c (H+)=c (HCO3-)+2 c (H2CO3) |
| C.加入少量NaOH固体,c (CO32―)与c (Na+)均增大 |
| D.c (Na+) > c (CO32―) > c (HCO3―) > c(OH―) > c (H+) |
① 钠比锂活泼,用原子结构解释原因_______。
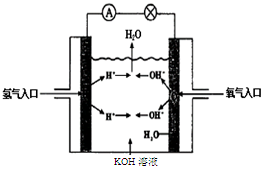
②ZEBRA 电池是一种钠电池,总反应为NiCl2 + 2Na
 Ni + 2NaCl。其正极反应式是_____。
Ni + 2NaCl。其正极反应式是_____。 

 2LiH Ⅱ.LiH+H2O=LiOH+H2↑
2LiH Ⅱ.LiH+H2O=LiOH+H2↑