题目内容
8.根据下列某些短周期元素中元素性质的有关句回答问题.| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |
| 原子半径/10 -10m | 0.37 | 1.86 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.52 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | +3 | +4 | +5 | +7 | +1 | +5 | ||
| 最低价态 | -1 | -2 | -4 | -3 | -1 | -3 | -1 |
(2)元素⑤、⑥和⑦的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质有CCl4、PCl3(写化学式).
(3)元素⑦离子的结构示意图
 .
.(4)元素①和⑨形成阳离子,其结构式为
 ,其中心原子以sp3杂化轨道成键.
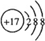
,其中心原子以sp3杂化轨道成键.(5)元素②和⑦形成晶体的部分结构可用图中的A来表示.元素⑤最高价氧化物的晶体结构可以用下图C来表示.(填序号)
分析 ①②⑧最高正价都是+1,处于ⅠA族,原子半径①<⑧<②,则①为H、②为Na、⑧为Li;⑦⑩都有最低价-1,则处于ⅦA族,⑩没有正化合价,⑦为Cl、⑩为F;⑥⑨都有最高正价+5,处于ⅤA族,原子半径⑥>⑨,则⑥为P、⑨为N;③只有最低负价-2,则③为O;④只有最高正价+3,处于ⅢA族,原子半径大于磷原子,则④为Al;⑤有最高正价+4、最低负价-4,处于ⅣA族,原子半径小于氯原子,则⑤为C,据此解答.
解答 解:①②⑧最高正价都是+1,处于ⅠA族,原子半径①<⑧<②,则①为H、②为Na、⑧为Li;⑦⑩都有最低价-1,则处于ⅦA族,⑩没有正化合价,⑦为Cl、⑩为F;⑥⑨都有最高正价+5,处于ⅤA族,原子半径⑥>⑨,则⑥为P、⑨为N;③只有最低负价-2,则③为O;④只有最高正价+3,处于ⅢA族,原子半径大于磷原子,则④为Al;⑤有最高正价+4、最低负价-4,处于ⅣA族,原子半径小于氯原子,则⑤为C.
(1)同周期自左而右电负性增大、同主族自上而下电负性减小,故电负性:F>Cl>Al>Na,
故答案为:F>Cl>Al>Na;
(2)元素C、N和Cl的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质是CCl4、PCl3,故答案为:CCl4、PCl3;
(3)元素⑦离子为Cl-,结构示意图为: ,故答案为:
,故答案为: ;
;
(4)元素①和⑨形成阳离子为NH4+,其结构式为 ,其中心N原子成4个N-H键,以sp3杂化轨道成键,故答案为:
,其中心N原子成4个N-H键,以sp3杂化轨道成键,故答案为: ;sp3;
;sp3;
(6)元素②和⑦形成晶体为NaCl,属于离子化合物,其晶胞结构中每个钠离子周围有6个氯离子、每个氯离子周围有6规格钠离子,A图符合其结构;
元素⑤最高价氧化物为CO2,属于分子晶体,为分子密堆积,每个分子周围有12个分子,图中C符合其结构,
故答案为:A;C.
点评 本题是对物质结构的考查,涉及元素周期表、电负性、核外电子排布、杂化轨道、晶胞结构等,难度中等,注意识记中学常见晶胞结构.

| A. | 苯酚 | B. | 二氧化硫 | C. | 氯化氢 | D. | 氯气 |
 (1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:
(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的热化学方程式为:a.C(s)+O2(g)═CO2(g)△H=E1①
b.C(s)+H2O(g)═CO(g)+H2(g)△H=E2②
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=E3③
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=E4④
请表达E1、E2、E3、E4之间的关系为E2=E1-E3-E4.
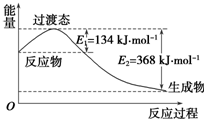
(2)如图所示是1摩尔NO2和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1.
(3)化学反应的焓变与反应物和生成物的键能有关.已知某些化学键的键能如下表所示:
| 共价键 | H-H | Cl-Cl | H-Cl |
| 键能/(kJ•mol-1) | 436 | 247 | 434 |
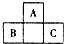 如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )
如图所示是元素周期表中短周期的一部分,已知B原子与C原子核外电子总数为A原子核外电子总数的4倍,则下列推断正确的是( )| A. | A、B、C三者均为非金属元素 | B. | B与C只能形成一种共价化合物 | ||
| C. | A与B、A与C均可形成离子化合物 | D. | A、B、C三者最外层电子数之和为40 |
| A. | 分子式为C5H12O且可与金属钠反应放出氢气的有机物有4种 | |
| B. | 甲苯分子中所有原子可能共面 | |
| C. | 苯、乙醇、油脂均不能使酸性KMnO4溶液褪色 | |
| D. | C3H2Cl6有四种同分异构体 |
| A. | KIO3 | B. | 苯甲酸钠 | C. | 维生素E | D. | NaNO2 |
| A. | 元素的非金属性:X>Y>Z | B. | 原子半径:X>Y>Z | ||
| C. | 气态氢化物稳定性:X<Y<Z | D. | 原子序数:Z>Y>X |
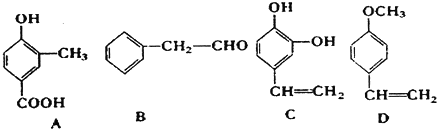
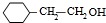 ;1molC最多能与3mol Br2发生反应.
;1molC最多能与3mol Br2发生反应. H
H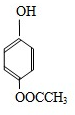 .G和NaOH溶液反应的化学方程式为
.G和NaOH溶液反应的化学方程式为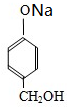 +HCOONa+H2O.
+HCOONa+H2O.