题目内容
拟晶Al65Cu23Fe12具有合金的某些优良物理性能,将相同质量的此拟晶分别与足量的盐酸、烧碱和稀硝酸反应,产生气体物质的量关系为( )
| A、n(盐酸)<n(稀硝酸)<n(烧碱) |
| B、n(烧碱)<n(盐酸)<n(稀硝酸) |
| C、n(烧碱)<n(稀硝酸)<n(盐酸) |
| D、n(稀硝酸)<n(烧碱)<n(盐酸) |
考点:化学方程式的有关计算
专题:
分析:将Al65Cu23Fe12看做65mol铝、23mol铜、12mol铁组成的混合物,Al和Fe能与稀盐酸反应、只有Al能和NaOH溶液反应、Cu和Al及Fe都可以和稀硝酸反应,据此计算.
解答:
解:将Al65Cu23Fe12看做65mol铝、23mol铜、12mol铁组成的混合物,Al和Fe能与稀盐酸反应、只有Al能和NaOH溶液反应、Cu和Al及Fe都可以和稀硝酸反应,
和NaOH溶液混合生成n(H2)=
×2=97.5mol;
与盐酸反应时,Al、Fe都反应,生成n(H2)=
×2+
×1=109.5mol;
与稀硝酸反应时三种金属都溶解放出NO气体,生成n(NO)=
×1+
+
×1=92.3mol;所以产生气体物质的量关系为n(稀硝酸)<n(烧碱)<n(盐酸),
故选D.
和NaOH溶液混合生成n(H2)=
| 65mol |
| 3 |
与盐酸反应时,Al、Fe都反应,生成n(H2)=
| 65mol |
| 3 |
| 12mol |
| 1 |
与稀硝酸反应时三种金属都溶解放出NO气体,生成n(NO)=
| 65mol |
| 1 |
| 23mol×2 |
| 3 |
| 12mol |
| 1 |
故选D.
点评:本题考查化学方程式的计算,侧重考查分析计算能力,采用转移电子守恒计算生成气体的物质的量,总结解题方法,题目难度中等.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
下列离子或分子在溶液中能大量共存,加入足量Na2O2后溶液中仍能大量共存的是( )
| A、K+、Cl-、Na+、SiO32- | ||
B、Ba2+、NO
| ||
| C、K+、Na+、I-、SO42- | ||
D、Na+、Cu2+、NH3.H2O、SO
|
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、在标准状况下,2.24 L HF含有的电子数为NA |
| B、7.8 g Na2S和Na2O2的混合物中所含离子数为0.3NA |
| C、常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
| D、电解精炼铜时,阳极质量每减少32 g,电路中就转移NA个电子 |
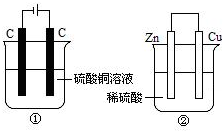 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )| A、产生气体体积 ①=② |
| B、①中阴极质量增加,②中正极质量减小 |
| C、溶液的pH变化:①减小,②增大 |
| D、电极反应式:①中阳极:4OH--4e-=2H2O+O2↑②中负极:2H++2e-=H2↑ |
下列说法正确的是( )
| A、能通过化合反应制得FeCl2和Fe(OH)3 |
| B、7.8gNa2O2与CO2完全反应,转移0.2mol电子 |
| C、Na、Fe分别与不足量的稀硫酸反应所得溶液均呈中性 |
| D、NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( )
| A、处理废水时加入明矾作为消毒剂可以除去水中的杂质 |
| B、为防止中秋月饼等富脂食品氧化变质,常在包装中放入生石灰 |
| C、金属汞一旦洒落在地面或桌面时,必须尽可能收集,并深埋处理 |
| D、高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 |
 将1.66g碳酸钠和氢氧化钠的固体混合物完全溶于水,配成稀溶液,然后向该溶液中逐滴加入1mo1?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示.
将1.66g碳酸钠和氢氧化钠的固体混合物完全溶于水,配成稀溶液,然后向该溶液中逐滴加入1mo1?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示. 某温度下,将三种气体充入一密闭容器中,所发生反应的平衡常数可表示为K=
某温度下,将三种气体充入一密闭容器中,所发生反应的平衡常数可表示为K=