题目内容
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、在标准状况下,2.24 L HF含有的电子数为NA |
| B、7.8 g Na2S和Na2O2的混合物中所含离子数为0.3NA |
| C、常温下,2.7 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
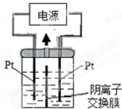
| D、电解精炼铜时,阳极质量每减少32 g,电路中就转移NA个电子 |
考点:阿伏加德罗常数
专题:
分析:A.气体摩尔体积适用对象为气体;
B.硫化钠和过氧化钠的摩尔质量相等,1mol过氧化钠中含有1mol阴离子;
C.铝与浓硫酸常温下发生钝化;
D.粗铜中含有杂质,电解过程中杂质铁、锌等优先放电,导致阳极溶解的铜减少.
B.硫化钠和过氧化钠的摩尔质量相等,1mol过氧化钠中含有1mol阴离子;
C.铝与浓硫酸常温下发生钝化;
D.粗铜中含有杂质,电解过程中杂质铁、锌等优先放电,导致阳极溶解的铜减少.
解答:
解:A.标准状况下,氢氟酸为液态,不能使用气体摩尔体积,故A错误;
B.1mol过氧化钠中含有1mol阴离子,7.8g Na2S和Na2O2的混合物中含有的离子数等于0.3NA,故B正确;
C.常温下,2.7 g铝片投入足量的浓硫酸中发生钝化,铝失去的电子数小于0.3NA,故C错误;
D.电解精炼铜时每转移NA个电子,转移了1mol电子,由于粗铜中含有较活泼的杂质Fe、Zn等,电解时杂质优先放电,所以阳极溶解的铜小于0.5mol,溶解的铜的质量小于32g,故D错误;
故选:B.
B.1mol过氧化钠中含有1mol阴离子,7.8g Na2S和Na2O2的混合物中含有的离子数等于0.3NA,故B正确;
C.常温下,2.7 g铝片投入足量的浓硫酸中发生钝化,铝失去的电子数小于0.3NA,故C错误;
D.电解精炼铜时每转移NA个电子,转移了1mol电子,由于粗铜中含有较活泼的杂质Fe、Zn等,电解时杂质优先放电,所以阳极溶解的铜小于0.5mol,溶解的铜的质量小于32g,故D错误;
故选:B.
点评:本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意气体摩尔体积适用对象和使用条件,题目难度不大.

练习册系列答案
相关题目
化学与生产、生活密切相关.下列叙述错误的是( )
| A、光导纤维和陶瓷都是硅酸盐产品 |
| B、晶体硅可用于制造芯片 |
| C、钢铁厂用热还原法冶炼铁 |
| D、焙制糕点的发酵粉主要成分之一是碳酸氢钠 |
25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O (l)△H=-285.8 kJ?mol-1 |
| B、2H2(g)+O2(g)=2H2O (l)△H=+571.6 kJ?mol-1 |
| C、2H2(g)+O2(g)=2H2O (g)△H=-571.6 kJ?mol-1 |
| D、H2(g)+1/2O2(g)=H2O (l)△H=-285.8 kJ?mol-1 |
拟晶Al65Cu23Fe12具有合金的某些优良物理性能,将相同质量的此拟晶分别与足量的盐酸、烧碱和稀硝酸反应,产生气体物质的量关系为( )
| A、n(盐酸)<n(稀硝酸)<n(烧碱) |
| B、n(烧碱)<n(盐酸)<n(稀硝酸) |
| C、n(烧碱)<n(稀硝酸)<n(盐酸) |
| D、n(稀硝酸)<n(烧碱)<n(盐酸) |
 甲、乙是两种氮的氧化物且所含元素价态均相同,某温度下相互转化时的量变关系如图所示.下列说法正确的是( )
甲、乙是两种氮的氧化物且所含元素价态均相同,某温度下相互转化时的量变关系如图所示.下列说法正确的是( )| A、甲是N2O4 |
| B、a点处于平衡状态 |
| C、t1~t2时间内v正(乙)<v逆(甲) |
| D、反应进行到t2时刻,改变的条件可能是升高温度 |


 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题: